题目内容
次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银.
①(H3PO2)中,磷元素的化合价为
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为: (填化学式);依据所学关于电镀的原理,分析该电镀过程中可选用的电极材料为阳极: ;阴极: .
③NaH2PO2是 (填“正盐”还是“酸式盐”),其溶液显 性(填“弱酸性”、“中性”、或者“弱碱性”),其溶液中离子浓度由大到小的顺序应
为
(3)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
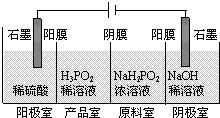
①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因 .
(1)H3PO2是一元中强酸,写出其电离方程式:
(2)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银.
①(H3PO2)中,磷元素的化合价为
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为:
③NaH2PO2是
为
(3)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因
考点:电解原理,氧化还原反应,弱电解质在水溶液中的电离平衡,盐类水解的原理
专题:
分析:(1)根据H3PO2是一元中强酸可知,H3PO2是弱电解质,溶液中部分电离出氢离子,据此写出电离方程式;
(2)①根据化合物中总化合价为0计算出P元素的化合价;
②先判断氧化剂、氧化剂,然后根据氧化剂与还原剂的物质的量之比为4:1计算出反应产物中P的化合价;根据H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银分析电极材料;
③根据H3PO2是一元中强酸,可以判断NaH2PO2为正盐;
(3)①根据阳极中阴离子为硫酸根离子、氢氧根离子和H2PO2-,判断放电能力强弱,然后写出阳极的电极反应式;
②根据图示“四室电渗析法”工作原理分析产品室可得到H3PO2的原因;
(2)①根据化合物中总化合价为0计算出P元素的化合价;
②先判断氧化剂、氧化剂,然后根据氧化剂与还原剂的物质的量之比为4:1计算出反应产物中P的化合价;根据H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银分析电极材料;
③根据H3PO2是一元中强酸,可以判断NaH2PO2为正盐;
(3)①根据阳极中阴离子为硫酸根离子、氢氧根离子和H2PO2-,判断放电能力强弱,然后写出阳极的电极反应式;
②根据图示“四室电渗析法”工作原理分析产品室可得到H3PO2的原因;
解答:
解:(1)H3PO2是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为H3PO2?H2PO2-+H+,故答案为:H3PO2?H2PO2-+H+;
(2)①H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价,故答案为:+1;
②该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;因为H3PO2可将溶液中的银离子还原为银单质,从而可用于化学镀银,所以阳极材料为石墨(惰性电极);阴极材料为待镀材料;故答案为:H3PO4;石墨(惰性电极);待镀材料;
③由于H3PO2是一元中强酸,所以NaH2PO2为一元强碱和一元中强酸形成的正盐,所以该盐溶液由于成H2PO2-发生水解成碱性,方程式为H2PO2-+H2O?H3PO2+OH-,所以溶液中离子浓度由大到小的顺序为c(Na+)>c(H2PO2-)>c(OH-)>c(H+);
故答案为:正盐;碱性;c(Na+)>c(H2PO2-)>c(OH-)>c(H+);
(3)①由于阳极中阴离子为硫酸根离子、氢氧根离子和H2PO2-,其中放电能力最强的是氢氧根离子,则阳极发生的电极反应为:4OH--4e-=O2↑+2H2O;故答案为:4OH--4e-=O2↑+2H2O;
②产品室可得到H3PO2的原因是因为:阳极室的H+穿过阳膜扩散至产品室,原料室的H2PO2-穿过阴膜扩散至产品室,二者反应生成H3PO2,
故答案为:阳极室的H+穿过阳膜扩散至产品室,原料室的H2PO2-穿过阴膜扩散至产品室,二者反应生成H3PO2;
(2)①H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价,故答案为:+1;
②该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;因为H3PO2可将溶液中的银离子还原为银单质,从而可用于化学镀银,所以阳极材料为石墨(惰性电极);阴极材料为待镀材料;故答案为:H3PO4;石墨(惰性电极);待镀材料;
③由于H3PO2是一元中强酸,所以NaH2PO2为一元强碱和一元中强酸形成的正盐,所以该盐溶液由于成H2PO2-发生水解成碱性,方程式为H2PO2-+H2O?H3PO2+OH-,所以溶液中离子浓度由大到小的顺序为c(Na+)>c(H2PO2-)>c(OH-)>c(H+);
故答案为:正盐;碱性;c(Na+)>c(H2PO2-)>c(OH-)>c(H+);
(3)①由于阳极中阴离子为硫酸根离子、氢氧根离子和H2PO2-,其中放电能力最强的是氢氧根离子,则阳极发生的电极反应为:4OH--4e-=O2↑+2H2O;故答案为:4OH--4e-=O2↑+2H2O;
②产品室可得到H3PO2的原因是因为:阳极室的H+穿过阳膜扩散至产品室,原料室的H2PO2-穿过阴膜扩散至产品室,二者反应生成H3PO2,
故答案为:阳极室的H+穿过阳膜扩散至产品室,原料室的H2PO2-穿过阴膜扩散至产品室,二者反应生成H3PO2;
点评:本题考查了盐的水解原理、弱电解质的电离、氧化还原反应等知识,题目难度中等,试题涉及的知识点较多,充分考查了学生对所学知识的掌握情况.

练习册系列答案
相关题目
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| B、已知2CO(g)+O2(g)?2CO2(g);△H=-akJ/mol,将2NA个CO与NA个O2混合充分反应放出akJ的热量 |
| C、用石灰乳完全吸收l mol Cl2时,转移电子的数目是NA |
| D、常温下,0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |
向Mg(HCO3)2溶液中加入NaOH溶液,可能出现的离子方程式为( )
| A、Mg2++2HCO3-+2OH-→MgCO3↓+CO32-+2H2O |
| B、Mg2++2HCO3-+2OH-→MgCO3↓+2H2O |
| C、Mg2++2HCO3-+4OH-→Mg(OH)2+2CO32-+2H2O |
| D、HCO3-+OH-→CO32-+2H2O |
卤代烃 C5H11Cl与C5H12O属于醇类的结构各有多少种( )
| A、5、3 | B、3、5 |
| C、10、8 | D、8、8 |
 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图: