题目内容
8.高铁酸钠是一种高效多功能水处理市.工业上常采用NaClO氧化法生产,反应原理是在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品.反应方程式为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O(1)上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是Na2FeO4在水溶液中易水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失.
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应方程式3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH.
分析 (1)Na2FeO4 为强碱弱酸盐,在水溶液中易水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解.
(2)负极是锌,失去电子在氢氧化钠的条件下生成氢氧化锌,高铁酸钠转化为氢氧化铁红褐色沉淀.
解答 解:(1)Na2FeO4 为强碱弱酸盐,在水溶液中易水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失,故答案为:Na2FeO4 为强碱弱酸盐,在水溶液中易水解后溶液呈碱性,NaOH溶液呈碱性会抑制其水解,有利于减少产品损失;
(2)负极是锌,失去电子在氢氧化钠的条件下生成氢氧化锌,高铁酸钠转化为氢氧化铁红褐色沉淀,电池反应为:3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH,故答案为:3Zn+2Na2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4NaOH.
点评 该题考查了学生盐类水解的基本知识,影响盐类水解的因素,正确书写电池反应方程式,难度不大,要求具有扎实的基本功.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
18.大枣等红色食物因富含铁,是很好的补铁食品.但因其中铁为Fe3+很难被人体直接吸收,需要食用富含维生素C的食物,将其转化为Fe2+,维生素C所具有的性质是( )
| A. | 氧化性 | B. | 还原性 | C. | 酸性 | D. | 碱性 |
19.将炼钛厂、氯碱厂和甲醇厂组成产业链如下,可得到烧碱、甲醇、钛以及其他一些有用的副产品.
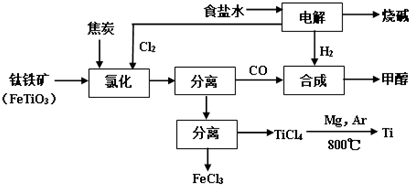
已知:合成甲醇的主反应为:CO+2H2?CH3OH+Q(Q>0,下同);
同时有副反应如:8CO+17H2?C8H18+8H2O+Q
4CO+8H2?C4H9OH+3H2O+Q.
请完成下列填空:
(1)在实验室电解饱和食盐水时,因工业食盐中含有少量氯化钙、硫酸镁等杂质,除杂时先加入沉淀剂,然后过滤,滤渣的成分是BaSO4、CaCO3、BaCO3、Mg(OH)2(填写化学式).
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;通电\;}}{\;}$2TiCl4+2FeCl3+6CO.
(3)诸如上述联合生产,其优点有大大提高资源利用率;降低生产成本;减少环境污染等.生产中除了获得上述目标产品外,还能得到副产品C8H18、C4H9OH、FeCl3、MgCl2(填写化学式).
(4)在上述产业链中,合成192吨甲醇理论上需额外补充H210吨(不考虑生产过程中物质的损失及副反应).
(5)上述产业链中“氯化”在600℃以上的反应器内进行.已知:
为了将TiCl4从“氯化”后的混合物中分离出来,请设计合理的方案:将氯化后的混合物冷却至1360C以下,使TiCl4和FeCl3均为液体;加热蒸馏混合液体,收集1360C的馏分.

已知:合成甲醇的主反应为:CO+2H2?CH3OH+Q(Q>0,下同);
同时有副反应如:8CO+17H2?C8H18+8H2O+Q
4CO+8H2?C4H9OH+3H2O+Q.
请完成下列填空:
(1)在实验室电解饱和食盐水时,因工业食盐中含有少量氯化钙、硫酸镁等杂质,除杂时先加入沉淀剂,然后过滤,滤渣的成分是BaSO4、CaCO3、BaCO3、Mg(OH)2(填写化学式).
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;通电\;}}{\;}$2TiCl4+2FeCl3+6CO.
(3)诸如上述联合生产,其优点有大大提高资源利用率;降低生产成本;减少环境污染等.生产中除了获得上述目标产品外,还能得到副产品C8H18、C4H9OH、FeCl3、MgCl2(填写化学式).
(4)在上述产业链中,合成192吨甲醇理论上需额外补充H210吨(不考虑生产过程中物质的损失及副反应).
(5)上述产业链中“氯化”在600℃以上的反应器内进行.已知:
| 物质 | 沸点(℃) |
| TiCl4 | 136 |
| FeCl3 | 315 |
16.有机化合物9,10-二甲基菲的结构如图所示.其苯环上七氯代物的同分异构体有( )
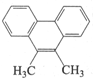

| A. | 8种 | B. | 5种 | C. | 4种 | D. | 3种 |
3.下列离子组在一定条件下能大量共存,且加入相应试剂后发生反应的离子方程式书写正确的是( )
| 选项 | 离子组 | 试剂 | 发生反应的离子方程式 |
| A | K+、AlO2-、NO3- | 过量CO2 | CO2+2H2O+AlO2-=Al(OH)3↓+HCO3- |
| B | Fe3+、I-、ClO- | 少量NaOH溶液 | Fe3++3OH-=Fe(OH) 3↓ |
| C | Ca2+、Na+、OH- | 少量NaHCO3溶液 | HCO3-+OH-=CO32-+H2O |
| D | NH4+、HCO3-、Cl- | 少量NaOH溶液 | NH4++OH-=NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
13.某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品可能是( )
| A. | 乙二醇 | B. | 乙醇 | C. | 乙醛 | D. | 丙三醇 |
20.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | O.lmol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| B. | 分子数目为0.1NA的N2和NH3混合气体,原子间含有的共用电子对数为0.3NA | |
| C. | 电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA | |
| D. | 常温常压下,4.4g乙醛所含σ键数目为0.7NA |
17.以下说法正确的是( )
| A. | 电子在原子核外排布时,总是尽先排在能量最高的电子层里 | |
| B. | 原子核外各电子层最多能容纳的电子数2n2,所以钾原子的M层有9个电子 | |
| C. | 稀有气体元素都形成了稳定的电子层结构,所以这些元素一定不存在化合态 | |
| D. | 在1~18号元素中,最外层电子数等于电子层数的元素有3种 |
18.化学与生活、环境、社会密切相关,下列有关说法中正确的是( )
| A. | pH在5.6~7.0之间的降水通常被称为酸雨 | |
| B. | 计算机硅芯片,光导纤维,普通玻璃都属于硅酸盐产品 | |
| C. | 汽车尾车中的氮氧化物、一氧化碳、SO2和可吸入颗粒物等严重污染大气 | |
| D. | 在食品袋中放入盛有硅胶、生石灰的透气小袋,可防止食物受潮、氧化变质 |