题目内容
18.化学与生活、环境、社会密切相关,下列有关说法中正确的是( )| A. | pH在5.6~7.0之间的降水通常被称为酸雨 | |
| B. | 计算机硅芯片,光导纤维,普通玻璃都属于硅酸盐产品 | |
| C. | 汽车尾车中的氮氧化物、一氧化碳、SO2和可吸入颗粒物等严重污染大气 | |
| D. | 在食品袋中放入盛有硅胶、生石灰的透气小袋,可防止食物受潮、氧化变质 |
分析 A.正常雨水的pH约为5.6,酸雨的pH小于5.6;
B.硅、二氧化硅分别为单质、氧化物,都不属于硅酸盐;
C.氮氧化物、硫氧化物和可吸入颗粒物是大气的主要污染物,是空气质量日报的内容,对人体有害;
D.硅胶、生石灰能够防止受潮,但是不能抗氧化.
解答 解:A.酸雨是指溶液pH小于5.6的雨水,正常雨水的pH约为5.6,二氧化硫、氮氧化物等物质是形成酸雨的重要物质,故A错误;
B.计算机硅芯片的材料为Si,光导纤维的主要成分为二氧化硅,均不是硅酸盐产品,而普通玻璃属于硅酸盐产品,故B错误;
C.汽车尾车中的氮氧化物、一氧化碳、SO2和可吸入颗粒物等是大气的主要污染物,严重危害人体健康,故C正确;
D.由于硅胶、氧化钙能够吸水,所以在食品袋中放入盛有硅胶、生石灰的透气小袋,可防止食物受潮,但是无法防止食物的氧化变质,故D错误;
故选C.
点评 本题考查较为综合,涉及酸雨、硅酸盐、氮气污染物等知识,题目难度不大,化学与生活,化学来源于生产、生活,也服务于生产、生活,在学习过程中要理论联系实际,能运用所学知识解决实际问题.

练习册系列答案
相关题目
9.CH3-CH2-OH和CH3-O-CH3互为( )
| A. | 同分异构体 | B. | 同素异形体 | C. | 同位素 | D. | 同系物 |
13.复盐M【K3Fe(A2B4)3•3H2O】可用于蓝色印刷和摄影,某小组同学将纯净的化合物M在一定条件下加热分解,对所得其他产物和固体产物进行实验和探究.
(1)Fe元素在周期表中的位置是第四周期第ⅤⅢ族,验证固体产物中存在钾元素的方法是做焰色反应实验,透过蓝色钴玻璃观察火焰的颜色呈紫色.
(2)经分析,所得其他产物由甲、乙和水蒸气组成,甲、乙转化关系如图(Ⅰ),转化时的能力变化如图(Ⅱ),已知A是形成化合物种类最多的元素,B是地壳中含量最多的元素,X、Y、甲、乙是含A、B两元素的单质或化合物,则化合物乙的电子式为 ,写出反应X+Y→甲的热化学方程式:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.6KJ/mol.
,写出反应X+Y→甲的热化学方程式:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.6KJ/mol.

(3)该小组同学已知固体产物中,铁元素不以三价形式存在,而盐也只有K2AB3,为了进一步确定复盐M的分解反应方程式,小组同学对固体产物进行定量测量.

判断KMnO4(其还原产物为无色Mn2+溶液)溶液与试样反应到达滴定终点的现象为当加入最后一滴酸性高锰酸钾溶液时试样由无色变化为紫红色且振荡半分钟内部变化.由以上实验数据的分析可知,加热后所得固体产物中除K2AB3外还含有什么物质?它们之间的物质的量之比为多少?请把你的结论填入表中(可以不填满或补充空格).
(4)通过以上结论,复盐M加热分解的反应方程式为2K3Fe(C2O4)3•3H2O$\frac{\underline{\;\;△\;\;}}{\;}$3K2CO3+Fe+FeO+5CO2↑+4CO↑+6H2O.
(5)已知KHA2B4溶液呈酸性,向10mL0.01mol•L-1的H2A2O4溶液滴加0.01mol•L-1KOH溶液V(mL),下列叙述正确的是①②③.
①当V<10mL时,反应的离子方程式为H2A2B4+OH-=HA2B4++H2O
②当V=10mL时,溶液中C(HA2B4+)>C(H+)>C(A2B42-)>C(H2A2B4)
③当V=amL时,溶液中离子浓度的关系为c(K+)=2c(A2B42-)+c(HA2B4-)
若V=bmL时,溶液中离子浓度的关系为:c(K+)=c(A2B42-)+c(HA2B4-)+c(H2A2B4),则a>b.
(1)Fe元素在周期表中的位置是第四周期第ⅤⅢ族,验证固体产物中存在钾元素的方法是做焰色反应实验,透过蓝色钴玻璃观察火焰的颜色呈紫色.
(2)经分析,所得其他产物由甲、乙和水蒸气组成,甲、乙转化关系如图(Ⅰ),转化时的能力变化如图(Ⅱ),已知A是形成化合物种类最多的元素,B是地壳中含量最多的元素,X、Y、甲、乙是含A、B两元素的单质或化合物,则化合物乙的电子式为
 ,写出反应X+Y→甲的热化学方程式:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.6KJ/mol.
,写出反应X+Y→甲的热化学方程式:C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.6KJ/mol.
(3)该小组同学已知固体产物中,铁元素不以三价形式存在,而盐也只有K2AB3,为了进一步确定复盐M的分解反应方程式,小组同学对固体产物进行定量测量.

判断KMnO4(其还原产物为无色Mn2+溶液)溶液与试样反应到达滴定终点的现象为当加入最后一滴酸性高锰酸钾溶液时试样由无色变化为紫红色且振荡半分钟内部变化.由以上实验数据的分析可知,加热后所得固体产物中除K2AB3外还含有什么物质?它们之间的物质的量之比为多少?请把你的结论填入表中(可以不填满或补充空格).
| 固体产物中的成分 | K2AB3 | … | ||
| 物质的量之比 | ||||
(5)已知KHA2B4溶液呈酸性,向10mL0.01mol•L-1的H2A2O4溶液滴加0.01mol•L-1KOH溶液V(mL),下列叙述正确的是①②③.
①当V<10mL时,反应的离子方程式为H2A2B4+OH-=HA2B4++H2O
②当V=10mL时,溶液中C(HA2B4+)>C(H+)>C(A2B42-)>C(H2A2B4)
③当V=amL时,溶液中离子浓度的关系为c(K+)=2c(A2B42-)+c(HA2B4-)
若V=bmL时,溶液中离子浓度的关系为:c(K+)=c(A2B42-)+c(HA2B4-)+c(H2A2B4),则a>b.
3.如表陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选 项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使酸性高锰酸钾褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可使纸张变黑 |
| D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
| A. | A | B. | B | C. | C | D. | D |
8.用惰性电极电解250mL NaCl和CuSO4的混合溶液,经过一段时间后,两电极分别得到11.2L气体(不考虑气体溶解),下列叙述中不正确的是( )
| A. | 阴极上有Cu析出 | |
| B. | 阴极上产生的气体是氢气 | |
| C. | 阳极上产生的气体是氯气和氧气混合气体 | |
| D. | 使溶液恢复到原来状态,需加人适量CuO并通适量HC1气体 |
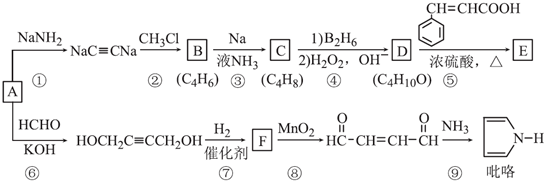
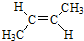 .
.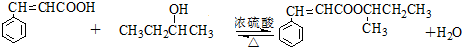 .
.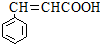 )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.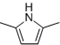 )的合成路线
)的合成路线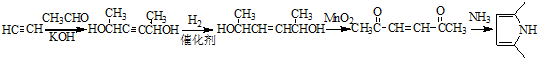 .
.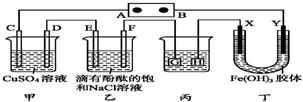 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.