题目内容
8.常温下,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中c(OH-)与c(H+)之比为1012,将两溶液等体积混合,以下判断正确的是( )| A. | HA是一种强酸 | B. | 反应后溶液中c(OH-)<c(H+) | ||
| C. | c(A-)>c(B+)>c(H+)>c(OH-) | D. | 反应后混合溶液中还含有HA分子 |
分析 常温下,0.1mol/L的酸HA溶液的pH>1,说明HA不完全电离,为弱电解质,0.1mol/L的碱BOH溶液中c(OH-)/c(H+)=1012,c(OH-).c(H+)=10-14,则c(OH-)=0.1mol/L,则BOH完全电离为强碱,将两溶液等体积混合,二者恰好反应生成强碱弱酸盐,溶液溶液呈碱性,据此进行解答.
解答 解:常温下,0.1mol/L的酸HA溶液的pH>1,说明HA不完全电离,为弱电解质,0.1mol/L的碱BOH溶液中c(OH-)/c(H+)=1012,c(OH-).c(H+)=10-14,则c(OH-)=0.1mol/L,则BOH完全电离为强碱,将两溶液等体积混合,二者恰好反应生成强碱弱酸盐,溶液溶液呈碱性,
A.常温下,0.1mol/L的酸HA溶液的pH>1,说明HA不完全电离为弱电解质,所以HA为弱酸,故A错误;
B.二者恰好反应生成强碱弱酸盐,弱酸根离子水解而使其溶液呈碱性,则c(OH-)>c(H+),故B错误;
C.二者恰好反应生成强碱弱酸盐,弱酸根离子水解而使其溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒可知c(A-)>c(B+),溶液中正确的离子浓度大小为:c(A-)>c(B+)>c(OH-)>c(H+),故C错误;
D.二者恰好反应生成强碱弱酸盐,弱酸根离子水解生成HA,所以溶液中还存在HA分子,故D正确;
故选D.
点评 本题考查了酸碱混合溶液定性判断,根据酸碱电离程度确定酸碱的强弱是解本题关键,再根据二者反应生成盐的性质来分析解答,难度中等.

练习册系列答案
相关题目
18.某同学在做锌与稀硫酸的反应,若稀硫酸足量,现欲加快化学反应速率,但不能影响生成氢气的总量,可采取的措施是( )
| A. | 加热 | B. | 滴入数滴硫酸铜溶液 | ||
| C. | 加入少量NaCl溶液 | D. | 加入少量KNO3溶液 |
19.已知自然界中氢的同位素有H、D、T三种,氯元素的同位素有 3517Cl和3717Cl两种,试估算自然界的氯化氢最多有( )
| A. | 2种 | B. | 3种 | C. | 6种 | D. | 9种 |
16.铅蓄电池是典型的可充电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:Pb+PbO2+2H2SO4$\frac{\underline{\;放电\;}}{充电}$2PbSO4+2H2O,有关该电池的说法正确的是( )
| A. | 放电时,负极质量减少 | |
| B. | 放电一段时间后,溶液的pH值减小 | |
| C. | 充电时,阳极反应:PbSO4+2e-=Pb+SO42- | |
| D. | 充电时,铅蓄电池的负极与外接电源的负极相连 |
3.下列反应中,属于加成的是( )
| A. | C2H5OH $→_{170℃}^{浓H_{2}SO_{4}}$ C2H4↑+H2O | |
| B. | 2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH | |
| C. | CH3-CH=CH2+Br2→CH3-CHBr-CH2Br | |
| D. |  +Br2 $\stackrel{Fe}{→}$ +Br2 $\stackrel{Fe}{→}$ 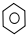 -Br+HBr -Br+HBr |
17.足量的铜与一定量的浓硝酸反应得到硝酸铜溶液和NO、NO2 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.则和铜反应的硝酸的物质的量可能是( )
| A. | 0.4mol | B. | 0.55mol | C. | 0.6mol | D. | 0.65mol |
18.盐酸具有的化学性质是( )
| A. | 酸性 | B. | 酸性、氧化性 | ||
| C. | 酸性、还原性 | D. | 酸性、氧化性、还原性 |