题目内容
16.硅是重要的无机非金属材料,工业上从硅的氧化物制取硅单质的主要反应为SiO2+2C═Si+2CO↑.其中,氧化剂是SiO2(填化学式),被氧化的物质是C(填化学式),若反应中消耗了0.4mol C,则生成0.2mol Si.分析 反应中Si元素化合价降低,被还原,SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,结合反应的化学方程式解答该题.
解答 解:反应中Si元素化合价降低,被还原,SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,由方程式可知,若反应中消耗了0.4mol C,则生成0.2mol Si.
故答案为:SiO2;C;0.2.
点评 本题考查氧化还原反应,为高考高频考点,侧重于化学与工业生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,注意从元素化合价的角度解答该题,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列关于环境、能源和材料的叙述中,错误的是( )
| A. | 光导纤维是以二氧化硅为主要原料制成的 | |
| B. | 在西部和沿海地区兴建风力发电站,解决能源短缺问题 | |
| C. | 糖类、油脂、蛋白质都属于天然有机高分子化合物 | |
| D. | 铁质器具表面刷漆或将其置于干燥处保存,均能有效减缓铁的锈蚀 |
13.下列有关碱土金属锶(Sr)元素单质及其化合物的叙述中,正确的是( )
| A. | 锶能与水反应,但反应缓慢 | B. | 硝酸锶是离子化合物,不溶于水 | ||
| C. | 氢氧化锶碱性弱于氢氧化镁的碱性 | D. | 金属锶单质银白色,导电性良好 |
4.一些科学家预言,存在稳定的超重元素,如:Z=114,N=184的原子,它位于元素周期表的第7周期,第ⅣA族,下列说法正确的是( )
| A. | 第七周期有50种元素 | B. | 该原子的质量数为184 | ||
| C. | 该元素的相对原子质量为298 | D. | 该原子核外有114个电子 |
11.An+、Bn-、C 3种短周期元素的粒子具有相同的电子层结构,则关于它们的叙述正确的是( )
| A. | 原子序数:C>B>A | B. | 离子半径:Bn-<An+ | ||
| C. | C是稀有气体元素的原子 | D. | 原子半径:A<B |
5.如图中的有机化合物可能发生的化学反应有( )

①加成 ②氧化 ③加聚 ④取代.

①加成 ②氧化 ③加聚 ④取代.
| A. | ①② | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
6.将含有0.4molNaCl和0.4molCu(NO3)2的水溶液1L用惰性电极电解一段时间后,在一个电极上析出0.3molCu,此时在另一个电极上放出气体的体积(标准状况)约为( )
| A. | 6.72L | B. | 5.6L | C. | 2.8L | D. | 13.44L |
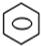 +HNO3(浓)$→_{50℃-60℃}^{浓硫酸}$
+HNO3(浓)$→_{50℃-60℃}^{浓硫酸}$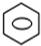 -NO2+H2O;取代反应
-NO2+H2O;取代反应