题目内容
7.已知,NO2和溴蒸汽都是红棕色气体,且都有强氧化性.在加压条件下,NO2可以发生如下反应:2NO2(g)?N2O4(g).下列试剂或方法中不能降NO2和溴蒸气区别开的是( )| A. | 向两种气体中加入适量水,震荡 | B. | 将两种气体分别通入AgNO3溶液中 | ||
| C. | 用湿润的淀粉KI试纸检验 | D. | 将两种气体加压、冷却 |
分析 二氧化氮和水反应生成硝酸和NO,而溴可溶于水,溴水呈橙黄色,可与硝酸银溶液反应生成浅黄色沉淀;二者都具有强氧化性,二者均与碱反应生成无色溶液,以此解答.
解答 解:A.溴水为橙黄色,二氧化氮溶于水为无色,可鉴别,故A正确;
B.二氧化氮通入到硝酸银溶液,有气体生成,而溴蒸气通入到硝酸银溶液中生成AgBr浅黄色沉淀,现象不同,能鉴别,故B正确;
C.NO2和Br2蒸气均能氧化KI中的碘离子生成碘单质,遇淀粉变蓝,现象相同,不能鉴别,故C错误;
D.将两种气体加压、冷却,红棕色液体为液溴,由2NO2(g)?N2O4(g)可知颜色变浅,现象不相同,能鉴别,故D正确;
故选C.
点评 本题考查物质的检验及鉴别,为高频考点,把握物质的性质、性质差异及发生的反应是解答本题的关键,侧重分析与应用能力的考查,选项D为解答的难点,题目难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
18.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,2.24L H2O中含有极性共价键的数目为0.2NA | |
| B. | 0.1mol•L-1 NH4Cl溶液中含有NH4+的数目小于0.1NA | |
| C. | 100mL 12mol•L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
15.如图是CO2生产甲醇的能量变化示意图.下列说法正确的是( )
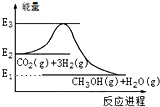

| A. | E2_E1是该反应的热效应 | |
| B. | E3_E1是该反应的热效应 | |
| C. | 该反应放热,在常温常压下就能进行 | |
| D. | 实现变废为宝,且有效控制温室效应 |
12.常温下0.1mol•L-1NaHSO3溶液,下列判断正确的是( )
| A. | 溶质的电离方程式为NaHSO3═Na++H++SO32- | |
| B. | c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-) | |
| D. | 加入少量NaOH固体,c(HSO3-)与c(Na+)均增大 |
8.如图所示为硝酸铜晶体[Cu(NO3)2•nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),从图中获取如下信息,不正确的有 ( )
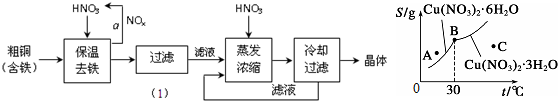

| A. | C点溶液为Cu(NO3)2的不饱和溶液 | |
| B. | 30℃时结晶可析出两种晶体 | |
| C. | 按上述流程最终得到的晶体是Cu(NO3)2•3H2O | |
| D. | 将A点溶液升温至30℃时,可以析出Cu(NO3)2•3H2O晶体. |
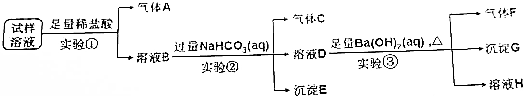
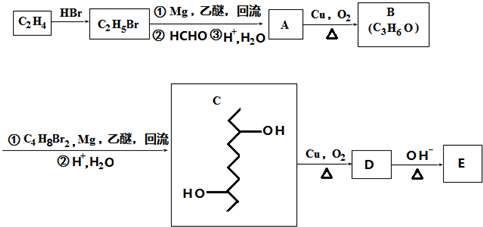
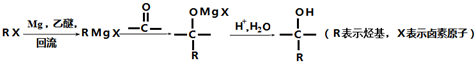

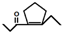 ,D在一定条件下转变为E的过程中还会生成另两种具有五元环结构的副产物,写出这两种副产物结构简式
,D在一定条件下转变为E的过程中还会生成另两种具有五元环结构的副产物,写出这两种副产物结构简式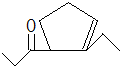 、
、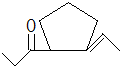 .
.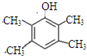 或
或