题目内容
7.下列说法正确的是( )| A | B | C | D |
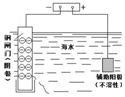
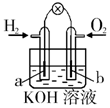
| 钢闸门容易被腐蚀 | a、b均为惰性电极,b极反应是:O+4OH--4e-=2H2O | 阴、阳两极生成的气体的物质的量之比是1:1 | 电池工作一段时间 后,乙池溶液的总质量增加 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A、金属的腐蚀与防护中如果有外接电源,此方法为外加电源的阴极保护法;
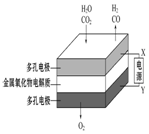
B、b极是氧气发生还原,电极反应式为:O2+4e-+2H2O=4OH-;
C、电解H2O-CO2混合气体制备H2和CO,总反应为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2,阴极产生H2、CO,阳极产生氧气,由此分析解答;
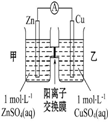
D、甲池中的Zn2+通过阳离子交换膜进入乙池,乙池中发生反应:Cu2++2e-=Cu,保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu.
解答 解:A、将钢闸门与外加电源负极相连,阴极上电解质溶液中阳离子得电子发生还原反应,此方法为外加电源的阴极保护法,可防止钢闸门腐蚀,故A错误;
B、b极是氧气发生还原,电极反应式为:O2+4e-+2H2O=4OH-,故B错误;
C、电解H2O-CO2混合气体制备H2和CO,总反应为:H2O+CO2$\frac{\underline{\;通电\;}}{\;}$H2+CO+O2,阴极产生H2、CO,阳极产生氧气,阴、阳两极生成的气体的物质的量之比是2:1,故C错误;
D、甲池中的Zn2+通过阳离子交换膜进入乙池,乙池中发生反应:Cu2++2e-=Cu,保持溶液呈电中性,进入乙池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu,故乙池溶液总质量增大,故D正确;
故选D.
点评 本题考查电解知识,为高频考点,侧重于考查学生的综合运用能力,题目难度中等,注意基础知识的积累掌握,掌握电解池阳极发生氧化反应,阳极发生氧化反应为解答关键.

练习册系列答案
相关题目
17. 5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:①A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3,沉淀部分溶解,剩余白色固体;②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、C的化学式为:ACuSO4;CBa(OH)2.
(2)写出步骤②中发生反应的化学方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)D溶液中滴入石蕊试液,现象是由无色变成红色,原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)步骤⑤中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(5)现用500mL 3mol•L-1的E溶液充分吸收11.2L CO2气体(标准状况 下),反应后溶液中各离子的物质量浓度由小到大的顺序为c(H+)<c(OH-)<c(CO32-)<c(HCO3-)<c(Na+).
(6)若用惰性电极电解A和B的混合溶液,溶质的物质的量均为0.1mol,请在坐标系中画出通电后阳极产生气体的体积(标准状况下)V与通过电子的物质的量n的关系(不考虑气体溶于水).
 5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.
5种固体物质A、B、C、D、E由表中不同的阴阳离子组成,它们均易溶于水.| 阳离子 | Na+ Al3+Fe3+ Cu2+、Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO4- |
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断A、C的化学式为:ACuSO4;CBa(OH)2.
(2)写出步骤②中发生反应的化学方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)D溶液中滴入石蕊试液,现象是由无色变成红色,原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式说明).
(4)步骤⑤中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(5)现用500mL 3mol•L-1的E溶液充分吸收11.2L CO2气体(标准状况 下),反应后溶液中各离子的物质量浓度由小到大的顺序为c(H+)<c(OH-)<c(CO32-)<c(HCO3-)<c(Na+).
(6)若用惰性电极电解A和B的混合溶液,溶质的物质的量均为0.1mol,请在坐标系中画出通电后阳极产生气体的体积(标准状况下)V与通过电子的物质的量n的关系(不考虑气体溶于水).
18.某校化学甲、乙两个小组学生利用下图所列装置进行“铁与水反应及相关性质”的实验.(图中夹持及尾气处理装置均已略去)
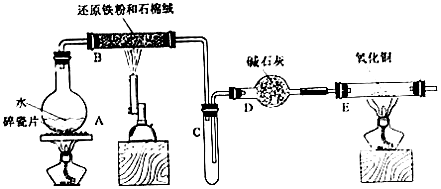
(1)烧瓶底部放置了几片碎瓷片,碎资片的作用是防暴沸.装置B中发生反应的化学方程式是3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4.
(2)如果要在E处玻璃管处点燃该气体,则必须对该气体进行验纯装置中的现象是黑色变为紫红色,试管口有水珠生成..
(3)将探究小组分为两组,按题图装置进行对比实验,甲组用洒精喷灯、乙组用洒精灯加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验.
①乙组得到的黑色粉末是FeO.
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Cl2+2Fe2+=2Fe3++2Cl-,Fe3++SCN-=FeSCN2+;溶液褪色可能的原因是氯水将SCN-氧化破坏了;验证方法为继续向溶液中滴入KSCN溶液,溶液变红即可证明.
(4)其中一组同学将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL.5mol•L-1FeSO4溶液和5.2g固体沉淀物,则原Fe2(SO4)3溶液的物质的量浓度为0.1mol/L;将沉淀物过滤后,该组同学又向清液中滴加稀硝酸,观察到有NO气体生成,发生的化学反应方程式为6FeSO4+8HNO3=2Fe2(SO4)3+2NO↑+4H2O+2Fe(NO3)3.

(1)烧瓶底部放置了几片碎瓷片,碎资片的作用是防暴沸.装置B中发生反应的化学方程式是3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4.
(2)如果要在E处玻璃管处点燃该气体,则必须对该气体进行验纯装置中的现象是黑色变为紫红色,试管口有水珠生成..
(3)将探究小组分为两组,按题图装置进行对比实验,甲组用洒精喷灯、乙组用洒精灯加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验.
| 步骤 | 操作 | 甲组现象 | 乙组现象 | |
| 1 | 取黑色粉末加入稀盐酸 | 洛解,无气泡 | 溶解,无气泡 | |
| 2 | 取少骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 | |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 | |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 | |
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Cl2+2Fe2+=2Fe3++2Cl-,Fe3++SCN-=FeSCN2+;溶液褪色可能的原因是氯水将SCN-氧化破坏了;验证方法为继续向溶液中滴入KSCN溶液,溶液变红即可证明.
(4)其中一组同学将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL.5mol•L-1FeSO4溶液和5.2g固体沉淀物,则原Fe2(SO4)3溶液的物质的量浓度为0.1mol/L;将沉淀物过滤后,该组同学又向清液中滴加稀硝酸,观察到有NO气体生成,发生的化学反应方程式为6FeSO4+8HNO3=2Fe2(SO4)3+2NO↑+4H2O+2Fe(NO3)3.
19. 亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
①2NO+Na2O2═2NaNO2
②2NO2+Na2O2═2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-被还原成Mn2+.
Ⅰ.产品制备与检验:用如图装置制备NaNO2
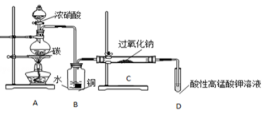
(1)写出装置A烧瓶中发生反应的化学方程式C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO);盛浓硝酸的仪器名称为分液漏斗.
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管.在干燥管中盛放的试剂名称为碱石灰.
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,滴加少量酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
(5)第一组实验数据出现异常,造成这种异常的原因可能是A、C.
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
 亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:①2NO+Na2O2═2NaNO2
②2NO2+Na2O2═2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-被还原成Mn2+.
Ⅰ.产品制备与检验:用如图装置制备NaNO2
(1)写出装置A烧瓶中发生反应的化学方程式C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO);盛浓硝酸的仪器名称为分液漏斗.
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管.在干燥管中盛放的试剂名称为碱石灰.
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,滴加少量酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
3.下列关于金属铝的叙述中,不正确的是( )
| A. | Al是地壳中含量最多的金属元素,但铝是使用较晚的金属 | |
| B. | Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性 | |
| C. | Al箔在空气中受热可以熔化,且发生剧烈燃烧 | |
| D. | Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al并不滴落 |
4.下列离子方程式中,属于水解反应的是( )
| A. | HCOOH+OH-═HCOO-+H2O | B. | CO2+H2O?ΗCΟ3-+H+ | ||
| C. | CO32-+H2O?ΗCΟ3-+OH- | D. | HS-+H2O?S2-+H3O+ |