题目内容
4.下列离子方程式中,属于水解反应的是( )| A. | HCOOH+OH-═HCOO-+H2O | B. | CO2+H2O?ΗCΟ3-+H+ | ||
| C. | CO32-+H2O?ΗCΟ3-+OH- | D. | HS-+H2O?S2-+H3O+ |
分析 A.为中和反应;
B.为碳酸的电离方程式;
C.碳酸根离子水解生成碳酸氢根离子和氢氧根离子;
D.为HS-的电离方程式.
解答 解:A.为醋酸与碱的中和反应,不是水解离子反应,故A不选;
B.二氧化碳与水结合生成碳酸,碳酸电离出碳酸氢根离子和氢离子,CO2+H2O?ΗCΟ3-+H+,故B不选;
C.碳酸根离子水解生成碳酸氢根离子和氢氧根离子,水解方程式为CO32-+H2O?ΗCΟ3-+OH-,故C选;
D.HS-的电离方程式为HS-+H2O?S2-+H3O+,水解方程式为HS-+H2O?H2S+OH-,故D不选;
故选C.
点评 本题考查盐类水解,为高频考点,把握水解原理和水解方程式的书写方法为解答的关键,侧重分析与应用能力的考查,注意水解原理的应用,题目难度不大.

练习册系列答案
相关题目
7.下列说法正确的是( )
| A | B | C | D |
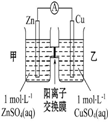
| 钢闸门容易被腐蚀 | a、b均为惰性电极,b极反应是:O+4OH--4e-=2H2O | 阴、阳两极生成的气体的物质的量之比是1:1 | 电池工作一段时间 后,乙池溶液的总质量增加 |
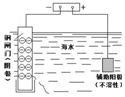 | 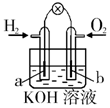 | 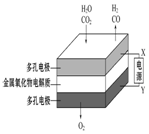 |  |
| A. | A | B. | B | C. | C | D. | D |
12.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 土壤胶体带负电荷,有利于铵态氮肥的吸收 | |
| B. | 加工后具有吸水性的植物纤维可用作食品干燥剂 | |
| C. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| D. | 燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
19.下列过程涉及化学变化的是( )
| A. | 食物腐败 | B. | 氨气液化 | C. | 海水晒盐 | D. | 石油分馏 |
9.下列说法不正确的是( )
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 加热、蒸发MgCl2饱和溶液可得无水MgCl2晶体 | |
| C. | 工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏 | |
| D. | 用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
13.下列叙述正确的是( )
| A. | 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀 | |
| B. | 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| C. | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失 | |
| D. | 纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率不改变快 |
14.下列关于实验的叙述,正确的是( )
| A. | 将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 | |
| B. | 除去苯中少量的苯酚:加溴水,振荡,过滤除去沉淀 | |
| C. | 只用溴水就可以将苯、四氯化碳、酒精、已烯、苯酚这五种物质区别开来 | |
| D. | 溴乙烷水解后的溶液中直接加入AgNO3溶液用来检验溴元素 |