题目内容
11.选用适当的试剂和方法除去下列物质中的杂质(括号内)填表:| 混合物 | 除杂质的试剂 | 除杂质的方法 |
| 苯(苯酚) | NaOH溶液 | 分液 |
| 酒精(水) | 生石灰 | 蒸馏 |
| 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
分析 苯酚与NaOH溶液反应后,与苯分层;
CaO与水反应后,增大与乙醇的沸点差异;
乙酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层,以此来解答.
解答 解:苯酚与NaOH溶液反应后,与苯分层,选择试试为NaOH溶液,然后分液分离;
CaO与水反应后,增大与乙醇的沸点差异,选择试剂为生石灰,然后蒸馏分离;
乙酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层,选择试剂为饱和碳酸钠溶液,然后分液分离,
故答案为:
| 混合物 | 除杂质的试剂 | 除杂质的方法 |
| 苯(苯酚) | NaOH溶液 | 分液 |
| 酒精(水) | 生石灰 | 蒸馏 |
| 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,注意有机物的性质应用,题目难度不大.

练习册系列答案
相关题目
1.在一定的温度下,在固定容积的密闭容器中,能表示反应X(气)+2Y(气)?2Z(气)一定达到化学平衡状态的是( )
①容器内压强不随时间改变; ②C(x)•C2(Y)=C2(z);③生成Z的速率与生成Y的速率相等; ④容器内混合气体的密度不随时间改变;⑤X、Y、Z的物质的量之比 1:2:2.
①容器内压强不随时间改变; ②C(x)•C2(Y)=C2(z);③生成Z的速率与生成Y的速率相等; ④容器内混合气体的密度不随时间改变;⑤X、Y、Z的物质的量之比 1:2:2.
| A. | ①③⑤ | B. | ①③ | C. | ②④ | D. | 全部 |
2.某气态烃0.5mol能和1mol HCl充分加成,加成产物1mol又能和6mol Cl2完全取代,则该烃是( )
| A. | C2H6 | B. | C2H2 | C. | C3H4 | D. | C4H6 |
19.下列有机物结构的表示方法不正确的是( )
| A. | 异戊烷的球棍模型: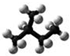 | B. | 乙醇的比例模型: | ||
| C. | 丙烯的结构简式:CH3CHCH2 | D. | 四氯化碳的电子式: |
6.下列粒子半径之比大于1的是( )
| A. | r(Al)/r(Na) | B. | r(C)/r(Si) | C. | r(F?)/r(Mg2+) | D. | r(Fe2+)/r(Fe) |
16.下列说法正确的是( )
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液变红 | |
| B. | 只存在共价键的物质一定是共价化台物、离子化合物中一定含有离子键 | |
| C. | Na2O与Na2O2组成元素相同、阴阳离子个数比相同,但跟水反应的产物不同 | |
| D. | 元素原子的最外层电子数越多,得电子能力越强,失电子能力越弱 |
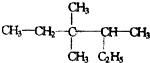 3,3,4-三甲基己烷
3,3,4-三甲基己烷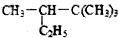 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷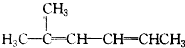 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯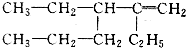 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.