题目内容
7.配制250mL 0.1mol•L-1的盐酸时,对于下列实验操作的叙述正确的是( )| A. | 用量筒量取所需的浓盐酸时俯视刻度线,则溶液的浓度偏低 | |
| B. | 定容时仰视刻度线,则溶液的浓度偏高 | |
| C. | 需选用250mL容量瓶,洗涤后残留少量蒸馏水,必须烘干后使用 | |
| D. | 定容后倒转容量瓶几次,发现液面最低点低于刻度线,需要再补几滴蒸馏水 |
分析 根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:A.用量筒量取所需的浓盐酸时俯视刻度线,则所量取的浓盐酸的体积偏小,配制出的溶液的浓度偏低,故A正确;
B.定容时仰视刻度线,则溶液体积偏大,浓度偏小,故B错误;
C.因洗涤容量瓶在定容操作之前,容量瓶用蒸馏水洗净后不影响溶液的体积,浓度不变,所以不需要干燥,故C错误;
D.定容后摇匀,发现液面最低点低于刻度线是正常的,再补加几滴蒸馏水至刻度线会导致浓度偏小,故D错误;
故选A.
点评 本题考查了配制一定物质的量浓度的溶液的误差分析,掌握c=$\frac{n}{V}$的理解应用是解答关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.将7.8g Na2O2和2.7g Al同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是( )
| A. | 反应过程中得到3.36L(标准状况)的气体 | |
| B. | 反应结束得到3.9g的沉淀 | |
| C. | 反应结束得到的溶液中含有AlCl3 | |
| D. | 反应结束得到的溶液中c(NaCl)═1.0 mol•L-1 |
15.下列分子的空间构型可用sp3杂化轨道来解释的是( )
①NF3 ②SO42- ③CH三CH ④CH4 ⑤H2O ⑥C6H6.
①NF3 ②SO42- ③CH三CH ④CH4 ⑤H2O ⑥C6H6.
| A. | ①②③⑥ | B. | ①②④⑤ | C. | ②③⑤⑥ | D. | ③④⑤⑥ |
2.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列关于MMF的说法正确的是( )
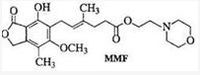

| A. | MMF能发生取代反应和消去反应 | |
| B. | 1 mol MMF能与6 mol 氢气发生加成反应 | |
| C. | 1 mol MMF能与含3 mol NaOH的水溶液完全反应 | |
| D. | MMF可与Na2CO3溶液反应生成气体 |
12.钠、铝、铁是中学化学常见的三种金属.下列说法中正确的是( )
| A. | 等物质的量的三种金属分别与足量的硫酸反应,金属钠放出H2最多 | |
| B. | 未经打磨的铝箔和经过打磨的铝箔,分别在酒精灯上加热至融化,前者融化不滴落,后者融化后滴落 | |
| C. | 铁表面的氧化膜是疏松的,不能保护内层的铁 | |
| D. | 钠跟氯化铜溶液反应,有红色沉淀生成 |
16.下列反应中的氨与反应4NH3+5O2=4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3═2NaNH2+H2↑ | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 4NH3+6NO═5N2+6H2O | D. | HCl+NH3═NH4Cl |
17.下列各组物质中,前者是单质,中间是氧化物,后者是混合物的是( )
| A. | 氯气、次氯酸钠、氯水 | B. | 木炭、二氧化硫、冰和水 | ||
| C. | 水银、氧化镁、氢氧化铁胶体 | D. | 钠、氧化钙、过氧化钠 |
