题目内容
3.下列实验中,所采取的分离方法不正确的是( )| 选项 | 目的 | 分离方法 |
| A | 除去铜器表面的铜绿【Cu2(OH)2CO3】 | 用盐酸浸泡,用清水冲洗 |
| B | 除去乙醇中的少量水 | 加生石灰,再蒸馏 |
| C | 除去 HCl中的 C12 | 通过饱和食盐水洗气再干燥 |
| D | 除去NaCl固 体中的 NH4Cl | 加热 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铜绿可与盐酸反应,而铜与盐酸不反应;
B.水与生石灰反应,可增大沸点差;
C.氯气不溶于饱和食盐水;
D.氯化铵不稳定,加热易分解.
解答 解:A.铜绿可与盐酸反应,而铜与盐酸不反应,可加入盐酸除杂,故A正确;
B.水与生石灰反应,可增大沸点差,可用蒸馏的方法分离,故B正确;
C.氯化氢乙溶于水,而氯气不溶于饱和食盐水,不能用饱和食盐水除杂,故C错误;
D.氯化铵不稳定,加热易分解,可用加热的方法分离,故D正确.
故选C.
点评 本题考查物质的分离、提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案
相关题目
13.设NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 常温下,pH=1的盐酸溶液中,由水电离的H+个数为10-13NA | |
| B. | 标准状况下,氧原子总数为0.2NA的CO2和NO2的混合气体,其体积为2.24L | |
| C. | 常温下,5.6g铁分别与足量氯气和稀硝酸反应,转移的电子数目均为0.3NA | |
| D. | 100g46%乙醇溶液中所含O-H数目为7NA |
8.获得“863”计划和中科院一百人计划支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,已知电池总反应为2Al+3I2═2AlI3.下列说法不正确的是( )
| A. | 该电池负极的电极反应为:Al-3e═Al3+ | |
| B. | 电池工作时,溶液中的铝离子向正极移动 | |
| C. | 消耗相同质量金属时,用锂做负极时,产生电子的物质的量比铝多 | |
| D. | 正极的电极材料是单质碘 |
12.实验室中电解饱和食盐水溶液时,不能直接得到的物质是( )
| A. | 氯化氢 | B. | 氢气 | C. | 氢氧化钠 | D. | 氯气 |
13.下列有关化学实验安全问题的叙述正确的是( )
| A. | 制备H2时,为防止H2逸出,待刚刚出现气泡时就在气体发生器出气口点燃 | |
| B. | 取用化学药品时,应特别注意药品包装容器上的安全警示标志 | |
| C. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| D. | 为更清楚地闻到化学药品的气味可使鼻子凑近药品 |
 在一定温度压强下,某反应在某体积为5L的密闭容器中进行,各物质的量的变化情况如图所示(A,B,C均为气体)
在一定温度压强下,某反应在某体积为5L的密闭容器中进行,各物质的量的变化情况如图所示(A,B,C均为气体) 有机物与人们的衣、食、住、行及健康等有非常密切的关系,认知和研究有机物具有十分重要的作用.
有机物与人们的衣、食、住、行及健康等有非常密切的关系,认知和研究有机物具有十分重要的作用.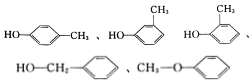 (任写一种).
(任写一种).