题目内容
将16g SO3加入ag水中,所形成的溶液中SO42-和水分子的个数比为1:5,则a 的值为( )
| A、90 | B、27 |
| C、21.6 | D、18 |
考点:化学方程式的有关计算
专题:计算题
分析:根据n=
计算SO3的物质的量,根据SO3+H2O=H2SO4计算反应消耗水的物质的量、生成硫酸物质的量,再计算形成的溶液中水的物质的量,进而计算水的总物质的量,根据m=nM计算水的质量.
| m |
| M |
解答:
解:16gSO3的物质的量为
=0.2mol,
SO3+H2O=H2SO4
0.2mol 0.2mol 0.2mol
形成的溶液中SO42-和水分子的个数比为1:5,则溶液中水的物质的量为0.2mol×5=1mol,
故水的总质量为:(1mol+0.2mol)×18g/mol=21.6g
故选C.
| 16g |
| 80g/mol |
SO3+H2O=H2SO4
0.2mol 0.2mol 0.2mol
形成的溶液中SO42-和水分子的个数比为1:5,则溶液中水的物质的量为0.2mol×5=1mol,
故水的总质量为:(1mol+0.2mol)×18g/mol=21.6g
故选C.
点评:本题考查物质的量有关计算,难度不大,属于易错题目,学生容易忽略参加反应水的质量.

练习册系列答案
相关题目
实验中需用2.0mol?L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为( )
| A、950 mL;201.4 g |
| B、1 000 mL;212.0 g |
| C、100 mL;21.2 g |
| D、500 mL;100.7 g |
已知1gH2完全燃烧生成水蒸气放出热量为121KJ,并且H-H键能为436KJ/mol,1molO=O键完全断裂时吸收的热量为496KJ,则形成1molH-O键放出的热量为( )
| A、436KJ |
| B、463KJ |
| C、649KJ |
| D、869KJ |
从1L1mol/L的NaOH溶液中,取出50mL溶液,该50mL NaOH溶液的物质的量浓度为( )
| A、0.02mol/L |
| B、0.2mol/L |
| C、1 mol/L |
| D、2mol/L |
N2、O2、CO2按体积比为1:2:3组成的混合气体共50g,在标准状况下的体积为( )
| A、60L | B、30L |
| C、11.2L | D、112L |
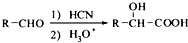 ,写出由C制备化合物
,写出由C制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH