题目内容
6.02×1024个Mg约含 mol Mg,其质量为 g;8克NH4NO3晶体中约含有 个N,共含有 molH原子.
考点:物质的量的相关计算
专题:计算题
分析:根据n=
=
结合物质的构成特点解答.
| N |
| NA |
| m |
| M |
解答:
解:n(Mg)=
=10mol,m(Mg)=10mol×24g/mol=240g,
n(NH4NO3)=
=0.1mol,
N(N)=0.1mol×2×NA/mol=0.2NA,
n(H)=0.4mol,
故答案为:10;240;0.2NA;0.4.
| 6.02×1024 |
| 6.02×1023/mol |
n(NH4NO3)=
| 8g |
| 80g/mol |
N(N)=0.1mol×2×NA/mol=0.2NA,
n(H)=0.4mol,
故答案为:10;240;0.2NA;0.4.
点评:本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
三聚氰胺的结构简式如图,下列说法不正确的是( )
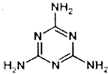

| A、三聚氰胺分子式C3N6H6,相对分子质量126 |
| B、已知合成三聚氰胺的反应是:6(NH2)CO→C3N6H6+6NH3+3CO2,反应物是尿素 |
| C、三聚氰胺分子所有原子在一个平面上 |
| D、三聚氰胺呈弱碱性,与盐酸、硫酸、硝酸、乙酸、草酸等都能形成三聚氰胺盐 |
某气体通入品红溶液,溶液褪色,加热后恢复红色,则该气体是( )
| A、N2 |
| B、SO2 |
| C、O2 |
| D、H2 |
将16g SO3加入ag水中,所形成的溶液中SO42-和水分子的个数比为1:5,则a 的值为( )
| A、90 | B、27 |
| C、21.6 | D、18 |
下列有关金属腐蚀与防护的说法正确的是( )
| A、在酸性环境下,钢铁只能发生析氢腐蚀 |
| B、金属腐蚀的实质是金属失去电子被还原的过程 |
| C、轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阳极的阴极保护法 |
| D、铜铁交接处,在潮湿的空气中直接发生反应:Fe-3e-═Fe3+,继而形成铁锈 |
下列叙述正确的是( )
| A、同温同压下,相同体积的气体,其分子数一定相等,原子数也一定相等 |
| B、任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 |
| C、同温同压下的一氧化碳气体和氮气,若体积相等,则质量一定相等 |
| D、1L一氧化碳气体一定比1L氧气的质量小 |
某元素的不同种同位素,这几种原子具有不同的( )
| A、质子数 | B、质量数 |
| C、核电荷数 | D、电子数 |