题目内容
 (1)25℃时,0.1mol?L-1的HA溶液中
(1)25℃时,0.1mol?L-1的HA溶液中| c(H+) |
| c(OH-) |
①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而减小的是
A.
| c(H+) |
| c(HA) |
| c(HA) |
| A- |
③若M溶液是由上述HA溶液V1mL与pH=12的NaOH溶液V2mL混合充分反应而得,则下列说法中正确的是
A.若溶液M呈中性,则溶液M中c(H+)+c(OH-)=2.0×10-7 mol?L-1
B.若V1=V2,则溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈碱性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp=1.8×10-10,现将足量AgCl分别放入:①100mL 蒸馏水中;②100mL 0.2mol?L-1 AgNO3溶液中;③100mL 0.1mol?L-1 AlCl3溶液中;④100mL 0.1mol?L-1盐酸中,充分搅拌后,相同温度下c(Ag+)由大到小的顺序是
(3)若1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1,单质硫的燃烧热为296kJ?mol-1,则由S(s)生成3mol SO3(g)的△H=
(4)对于2NO2(g)═N2O4(g)△H<0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.则下列说法正确的是
①A、C两点的反应速率:A>C
②A、C两点气体的颜色:A深、C浅
③B、C两点的气体的平均分子质量:B<C
④由状态B到状态A,可以用加热方法
(5)若利用甲烷燃料电池电解50mL 2mol?L-1的氯化铜溶液,请回答:甲烷燃料电池的负极反应式是
(6)室温下NaHCO3溶液的pH
考点:弱电解质在水溶液中的电离平衡,化学电源新型电池,化学平衡的影响因素,酸碱混合时的定性判断及有关ph的计算
专题:化学平衡专题,电离平衡与溶液的pH专题,电化学专题
分析:(1)①25℃时,0.1mol?L-1的某酸HA中,如果该酸是强酸,则
=1012,实际上则
=1010,所以该酸是弱酸,弱酸中存在电离平衡;根据BOH的pH计算出溶液中的氢氧根离子浓度,然后判断电解质强弱;
②加水稀释促进酸电离,氢离子浓度、酸浓度、酸根离子浓度都降低,但氢氧根离子浓度增大,注意水的离子积常数只与温度有关,与溶液的酸碱性无关;
③A.若混合溶液呈中性,则氢离子浓度等于氢氧根离子浓度;
B.如果二者体积相等,根据酸的强弱判断混合溶液的酸碱性;
C.如果溶液呈酸性,则溶液可能是酸和盐溶液;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液;
(2)氯化银饱和溶液中存在沉淀溶解平衡,饱和溶液中的溶度积是常数,只随温度变化;依据溶度积分别计算;
(3)根据反应2SO2(g)+O2(g)=2SO3(g)结合1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1计算反应热;
(4)N2O4(g)═2NO2(g)△H<0,该反应为吸热反应,升高温度,化学平衡正向移动,NO2的体积分数增大;增大压强,化学平衡逆向移动,NO2的体积分数减小,结合图象来分析解答,
①C两点都在等温线上,压强越大,反应速率越快;
②压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大,A点NO2的体积分数大;
③由图象可知,B、C两点NO2的体积分数相同,则气体的物质的量相同,据此判断;
④根据温度和压强对反应速率的影响来回答;
(5)原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+;正极氧气反应生成水;
(6)碳酸氢钠是强碱弱酸盐其溶液呈碱性,根据物料守恒及电荷守恒分析解答.
| c(H+) |
| c(OH-) |
| c(H+) |
| c(OH-) |
②加水稀释促进酸电离,氢离子浓度、酸浓度、酸根离子浓度都降低,但氢氧根离子浓度增大,注意水的离子积常数只与温度有关,与溶液的酸碱性无关;
③A.若混合溶液呈中性,则氢离子浓度等于氢氧根离子浓度;
B.如果二者体积相等,根据酸的强弱判断混合溶液的酸碱性;
C.如果溶液呈酸性,则溶液可能是酸和盐溶液;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液;
(2)氯化银饱和溶液中存在沉淀溶解平衡,饱和溶液中的溶度积是常数,只随温度变化;依据溶度积分别计算;
(3)根据反应2SO2(g)+O2(g)=2SO3(g)结合1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1计算反应热;
(4)N2O4(g)═2NO2(g)△H<0,该反应为吸热反应,升高温度,化学平衡正向移动,NO2的体积分数增大;增大压强,化学平衡逆向移动,NO2的体积分数减小,结合图象来分析解答,
①C两点都在等温线上,压强越大,反应速率越快;
②压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大,A点NO2的体积分数大;
③由图象可知,B、C两点NO2的体积分数相同,则气体的物质的量相同,据此判断;
④根据温度和压强对反应速率的影响来回答;
(5)原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+;正极氧气反应生成水;
(6)碳酸氢钠是强碱弱酸盐其溶液呈碱性,根据物料守恒及电荷守恒分析解答.
解答:
解:(1)①25℃时,0.1mol?L-1的某酸HA中,如果该酸是强酸,氢离子浓度为0.1mol/L,氢氧根离子浓度为:10-13mol/L,则
=1012>1010,所以该酸是弱酸;故答案为:弱电解质;
②A.加水稀释促进了弱酸的电离,溶液中氢离子的物质的量增大,HA的物质的量减小,相同溶液中:
,所以其比值增大,故A错误;
B.加水稀释促进酸电离,酸浓度、酸根离子浓度都降低,但酸根离子浓度减小的量小于酸分子减小的量,所以氢氧根离子浓度增大,则
减小,故B正确;
C.c(H+)与c(OH-)的乘积为水的离子积,温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,故D错误;
故答案为:B;
③A.若混合溶液呈中性,则溶液M中c(H+)=c(OH-)=1×10-7 mol?L-1,所以溶液M中c(H+)+c(OH-)=2×10-7 mol?L-1,故A正确;
B.若V1=V2,则酸的浓度大,酸过量,则溶液M的pH一定小于7,故B错误;
C.如果溶液呈酸性,则溶液是酸和盐溶液,酸是弱酸,酸浓度大于氢氧化钠浓度,所以V1不一定大于V2,故C错误;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液,则V1一定小于V2,故D正确;
故答案为:AD;
(2)氯化银饱和溶液中存在沉淀溶解平衡,氯离子浓度越大,则银离子浓度越小,
①100mL蒸馏水中氯化银形成饱和溶液,Ag+浓度为
×10-5mol/l;
②100mL 0.2mol?L-1AgNO3溶液中Ag+浓度为0.2mol/l抑制沉淀溶解平衡,
③100mL 0.1mol?L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;
④100mL 0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;
综上所述大小顺序为:②>①>④>③,
故答案为:②>①>④>③;
(3)已知①S(s)+O2(g)=SO2(g)△H1=-296 KJ?mol-1,②SO2(g)+
O2(g)=SO3(g)△H2=-99 KJ?mol-1;
则利用盖斯定律将①×3+②×3可得3 S(s)+
O2(g)=3SO3(g)△H3=3×(△H1+△H2)=-1185 KJ?mol-1,
故答案为:-1185 KJ?mol-1;
(4)①由图象可知,A、C两点都在等温线上,C的压强大,则A、C两点的反应速率:A<C,故①错误;
②A、C两点温度相同,但压强不同,NO2为红棕色气体,由图象可知,A点NO2的体积分数大,则A、C两点气体的颜色:A深,C浅,故②错误;
③由图象可知,B、C两点NO2的体积分数相同,则气体的物质的量相同,所以平均相对分子质量相同,故③错误;
④升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,故④正确;
故答案为:④;
(5)原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+,正极氧气得电子生成水,正极电极反应式为::2O2+8e-+8H+=4H2O,
故答案为:CH4-8e-+2H2O=CO2+8H+;2O2+8e-+8H+=4H2O;
(6)碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子易水解而导致其溶液呈碱性,碳酸氢根离子既能电离又能水解,但水解程度大于电离程度,其电离程度和水解程度都减小,钠离子不水解,且碳酸氢根离子水解和水电离都生成氢氧根离子,所以离子浓度大小顺序是C(Na+)>C(HCO3-)>C(OH-)>C(H+)>C(CO32-),
故答案为:>;HCO3-+H2O?H2CO3+OH-; C(Na+)>C(HCO3-)>C(OH-)>C(H+)>C(CO32-).
| c(H+) |
| c(OH-) |
②A.加水稀释促进了弱酸的电离,溶液中氢离子的物质的量增大,HA的物质的量减小,相同溶液中:
| n(H+) |
| n(HA) |
B.加水稀释促进酸电离,酸浓度、酸根离子浓度都降低,但酸根离子浓度减小的量小于酸分子减小的量,所以氢氧根离子浓度增大,则
| c(HA) |
| c(A-) |
C.c(H+)与c(OH-)的乘积为水的离子积,温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,故D错误;
故答案为:B;
③A.若混合溶液呈中性,则溶液M中c(H+)=c(OH-)=1×10-7 mol?L-1,所以溶液M中c(H+)+c(OH-)=2×10-7 mol?L-1,故A正确;
B.若V1=V2,则酸的浓度大,酸过量,则溶液M的pH一定小于7,故B错误;
C.如果溶液呈酸性,则溶液是酸和盐溶液,酸是弱酸,酸浓度大于氢氧化钠浓度,所以V1不一定大于V2,故C错误;
D.如果溶液呈碱性,则溶液可能是碱和盐溶液,也可能只是盐溶液,则V1一定小于V2,故D正确;
故答案为:AD;
(2)氯化银饱和溶液中存在沉淀溶解平衡,氯离子浓度越大,则银离子浓度越小,
①100mL蒸馏水中氯化银形成饱和溶液,Ag+浓度为
| 1.8 |
②100mL 0.2mol?L-1AgNO3溶液中Ag+浓度为0.2mol/l抑制沉淀溶解平衡,
③100mL 0.1mol?L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;
④100mL 0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;
综上所述大小顺序为:②>①>④>③,
故答案为:②>①>④>③;
(3)已知①S(s)+O2(g)=SO2(g)△H1=-296 KJ?mol-1,②SO2(g)+
| 1 |
| 2 |
则利用盖斯定律将①×3+②×3可得3 S(s)+
| 9 |
| 2 |
故答案为:-1185 KJ?mol-1;
(4)①由图象可知,A、C两点都在等温线上,C的压强大,则A、C两点的反应速率:A<C,故①错误;
②A、C两点温度相同,但压强不同,NO2为红棕色气体,由图象可知,A点NO2的体积分数大,则A、C两点气体的颜色:A深,C浅,故②错误;
③由图象可知,B、C两点NO2的体积分数相同,则气体的物质的量相同,所以平均相对分子质量相同,故③错误;
④升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,故④正确;
故答案为:④;
(5)原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+,正极氧气得电子生成水,正极电极反应式为::2O2+8e-+8H+=4H2O,
故答案为:CH4-8e-+2H2O=CO2+8H+;2O2+8e-+8H+=4H2O;
(6)碳酸氢钠是强碱弱酸酸式盐,碳酸氢根离子易水解而导致其溶液呈碱性,碳酸氢根离子既能电离又能水解,但水解程度大于电离程度,其电离程度和水解程度都减小,钠离子不水解,且碳酸氢根离子水解和水电离都生成氢氧根离子,所以离子浓度大小顺序是C(Na+)>C(HCO3-)>C(OH-)>C(H+)>C(CO32-),
故答案为:>;HCO3-+H2O?H2CO3+OH-; C(Na+)>C(HCO3-)>C(OH-)>C(H+)>C(CO32-).
点评:本题考查较为综合,涉及弱电解质的电离、化学平衡的影响因素、酸碱混合溶液的计算、电化学、离子浓度大小比较以及盖斯定律的应用等,题目难度中等,注意体会盖斯定律的应用,把握燃料电池中电极方程式的书写.

练习册系列答案
相关题目
常温下,将乙酸和氢氧化钠溶液混合,所得溶液 pH>7,则此溶液中( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COO-)<c(Na+) |
| C、c(CH3COO-)=c(Na+) |
| D、无法确定c(CH3COO-)与c(Na+)的关系 |
下列说法正确的是( )
| A、在潮湿的环境中,铜容易发生析氢腐蚀形成铜绿 |
| B、常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C、亚硫酸氢钠溶液显酸性:NaHSO3=Na++H++SO32- |
| D、对于Ca(OH)2的沉淀溶解平衡,升高温度,Ca(OH)2的溶解速率增大,Ksp减小 |
25℃时,几种弱酸的电离常数如下:25℃时,下列说法正确的是( )
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A、等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN) |
| B、a mol/LHCN溶液与b mol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于或等于b |
| C、NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
| D、某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-dmol/L |
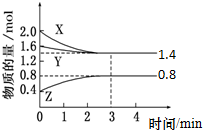 t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )
t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )| A、0~3 min,X的平均反应速率v(X)=0.1 mol?L-1?min-1 |
| B、发生反应的方程式可表示为:3 X(g)+Y(g)?2 Z(g) |
| C、3 min 时,Y的转化率为12.5%,此时,充入惰性气体Ne,转化率不变 |
| D、温度不变,增大Z的浓度,该反应的平衡常数增大 |
 2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德?埃特尔.他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论.在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示.下列说法正确的是( )
2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德?埃特尔.他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论.在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示.下列说法正确的是( )| A、NO2是该过程的中间产物 |
| B、NO和O2必须在催化剂表面才能反应催化剂 |
| C、汽车尾气的主要污染成分是CO2和NO |
| D、该催化转化的总反应方程式为:2NO+O2+4CO═4CO2+N2 |
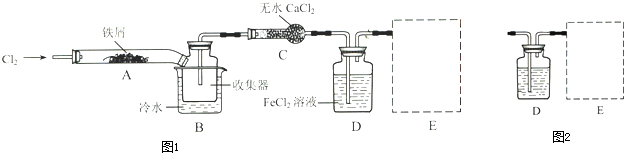
 氯气是一种重要的化工原料.如图为实验室制取氯气的装置.请回答:
氯气是一种重要的化工原料.如图为实验室制取氯气的装置.请回答: