题目内容
2.化学上将质量数相同而质子数不同的原子称为同量素,如40K和40Ca.下列关于40K和40Ca的叙述中正确的是( )| A. | 40K和40Ca 具有相同的中子数 | |
| B. | 40K+和40Ca2+ 具有相同的电子层结构 | |
| C. | 39K和40Ca互为同位素 | |
| D. | 40K的原子半径小于40Ca 的原子半径 |
分析 A.根据原子符号的含义、质子数=原子序数以及中子数=质量数-质子数;
B.根据离子的结构示意图来分析;
C.质子数相同中子数不同的同一元素互称同位素;
D.同周期从左到右原子半径依次减小.
解答 解:A.40K和40Ca 的原子序数分别为19、20,则质子数分别为19、20、中子数分别为40-19=21,40-20=20,中子数不相同,故A错误;
B.40K+和40Ca2+离子的结构示意图分别 、
、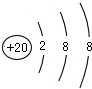 ,电子层结构相同,故B正确;
,电子层结构相同,故B正确;
C.40K和40Ca的质子数不同,所以两者不是同位素,故C错误;
D.同周期从左到右原子半径依次减小,40K的原子半径大于40Ca 的原子半径,故D错误;
故选B;
点评 本题主要考查了原子符号的含义、离子的结构示意图、同素异形体、同位素等,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
12.下列物质中,在该状态下能够导电的电解质是( )
| A. | Fe片 | B. | 蔗糖 | C. | 固体NaCl | D. | 熔融的CuCl2 |
13.除去下列括号内杂质的试剂或方法错误的是( )
| A. | 溴苯(Br2):加水,萃取分液 | B. | SiO2(Fe2O3):足量的盐酸,过滤 | ||
| C. | Cl2(HCl):通过饱和氯化钠溶液 | D. | C2H5OH(CH3COOH):加足量CaO,蒸馏 |
10.有机化合物与人类的生活密切相关.以下叙述中,正确的是( )
①乙醇和乙酸都是常用调味品的主要成分 ②米酒变酸的过程涉及了氧化反应
③含磷合成洗涤剂易于被细菌分解,故不会导致水污染
④有机酸和醇脱水合成的某些酯,可用作糖果、化妆品中的香料
⑤用加酶洗衣粉洗涤毛织品效果更好.
①乙醇和乙酸都是常用调味品的主要成分 ②米酒变酸的过程涉及了氧化反应
③含磷合成洗涤剂易于被细菌分解,故不会导致水污染
④有机酸和醇脱水合成的某些酯,可用作糖果、化妆品中的香料
⑤用加酶洗衣粉洗涤毛织品效果更好.
| A. | ②③⑤ | B. | ①②④ | C. | ①②③ | D. | ①④⑤ |
17.(1)已知2H2+O2═2H2O的反应反应为放热反应,如图能正确表示该反应中能量变化的是A(填编号).
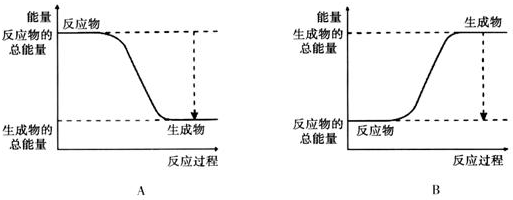
(2)若从断键和成键的角度分析上述反应中能量的变化.化学键的键能如表:
则生成1mol水放出的热量为242kJ.

(2)若从断键和成键的角度分析上述反应中能量的变化.化学键的键能如表:
| 化学键 | H-H | O═O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
7.去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示.下列说法正确的是( )
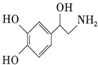

| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 去甲肾上腺素属于氨基酸 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
2.主族元素在周期表中的位置取决于元素原子的( )
| A. | 质量数和核外电子数 | B. | 质量数和最外层电子数 | ||
| C. | 电子层数和最外层电子数 | D. | 电子层数和中子数 |
3.下列化学用语书写正确的是( )
| A. | 丙烯的键线式: | B. | 羟基的电子式: | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 乙炔的结构式H-C≡C-H |
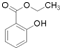 )广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下:
)广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下: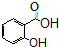 +C2H5OH?
+C2H5OH?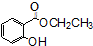 +H2O
+H2O