题目内容
4.白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列化学键需要吸收的能量分别为:| P-P | P-O | P=O | O=O | |
| 键能 (kJ/mol) | a | b | c | d |
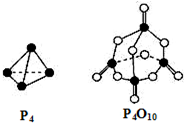
根据图所示的分子结构和有关数据计算该反应的△H,其中正确的是( )
| A. | (4c+12b-6a-5d)kJ•mol-1 | B. | (6a+5d-4c-12b)kJ•mol-1 | ||
| C. | (4c+12b-4a-5d)kJ•mol-1 | D. | (4a+5d-4c-12b)kJ•mol-1 |
分析 反应热△H=反应物总键能-生成物总键能,据此计算判断.注意每摩尔P4中含有6molP-P键.
解答 解:各化学键键能为P-P a kJ•mol-1、P-O b kJ•mol-1、P=O c kJ•mol-1、O=O d kJ•mol-1.
反应热△H=反应物总键能-生成物总键能,
所以反应P4+5O2=P4O10的反应热△H=6akJ•mol-1+5dkJ•mol-1-(4ckJ•mol-1+12bkJ•mol-1)=(6a+5d-4c-12b)kJ•mol-1,
故选:B.
点评 本题考查反应热与化学键键能的关系,难度中等,注意从物质能量、键能理解反应热.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
14.除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是( )
| A. | FeCl2溶液(FeCl3):Fe粉 | B. | CO2(SO2):饱和的Na2CO3溶液 | ||
| C. | Al2O3(SiO2):NaOH溶液 | D. | Cl2(HCl):NaOH溶液 |
15.研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
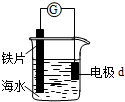

| A. | d为石墨,电流从d流入导线进入铁片 | |
| B. | d为铜片,铜片上电极反应为:O2+2H2O+4e-═4OH- | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为镁片,铁片上电极反应为:2H++2e-═H2↑ |
12.能用如图装置进行喷泉实验的气体是( )


| A. | CO2 | B. | CO | C. | O2 | D. | NO |
19.下列推断正确的是( )
| A. | 由H+(aq)+OH- (aq)═H2O(l);△H=-57.3 kJ•mol-1:可知含1 mol氢氧化钡的溶液与含0.5 mol硫酸的稀溶液混合,放出热量大于57.3 kJ | |
| B. | 由H2O(g)═H2O(l)△H=-44.0kJ•mol-1可知是放热反应 | |
| C. | 由SO2(g)+0.5O2(g)═SO3(g)△H=-98.3 kJ•mol-1可知,在密闭容器中充入2 mol SO2和1 mol O2充分反应后,放出热量为196.6 kJ | |
| D. | 由△G=△H-T△S可知,所有放热反应都能自发进行 |
13.在恒容的密闭容器中,一定温度下可逆反应A(g)+3B(g)?2C(g)达到化学反应平衡的标志是( )
| A. | 单位时间内消耗n molA,同时消耗3n mol B | |
| B. | A、B、C三者的浓度相同 | |
| C. | 容器内气体的压强不随时间的变化而变化 | |
| D. | 混合气体的密度不在发生变化 |
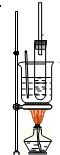 实验室制取硝基苯的方法如图所示:
实验室制取硝基苯的方法如图所示: ,
,