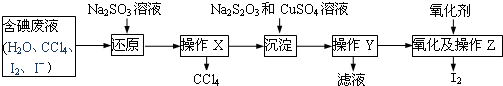
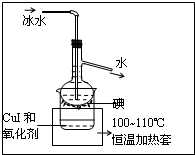
题目内容
15.研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )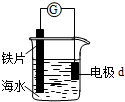
| A. | d为石墨,电流从d流入导线进入铁片 | |
| B. | d为铜片,铜片上电极反应为:O2+2H2O+4e-═4OH- | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为镁片,铁片上电极反应为:2H++2e-═H2↑ |
分析 A、d为石墨,铁片活泼,电流由正极沿导线流向负极;
B、海水呈中性,所以发生吸氧腐蚀;
C、锌比铁片活泼,所以腐蚀锌;
D、d为锌块,作为负极,因海水呈中性,所以发生吸氧腐蚀.
解答 解:A、d为石墨,活泼金属铁片作负极,电流从d流入导线进入铁片,故A正确;
B、海水呈中性,所以发生吸氧腐蚀,所以石墨作正极,电极反应:O2+2H2O+4e═4OH-,故B正确;
C、锌比铁片活泼,所以腐蚀锌,所以铁片不易被腐蚀,故C正确;
D、d为锌块,作为负极,因海水呈中性,所以发生吸氧腐蚀,所以铁片上电极反应为:O2+2H2O+4e═4OH-,故D错误;
故选D.
点评 本题考查了原电池原理,根据电极上得失电子判断正负极,再结合电极反应类型、电子流向来分析解答,熟记原电池原理,难点是电极反应式的书写.

练习册系列答案
相关题目
6.Zn还原SiCl4的反应如下:
SiCl4(g)+2Zn(l)?Si(s)+2ZnCl2(g)△H1
SiCl4(g)+2Zn(g)?Si(s)+2ZnCl2(g)△H2
下列说法正确的是( )
SiCl4(g)+2Zn(l)?Si(s)+2ZnCl2(g)△H1
SiCl4(g)+2Zn(g)?Si(s)+2ZnCl2(g)△H2
下列说法正确的是( )
| A. | Zn(l)=Zn(g)△H=$\frac{1}{2}$(△H1-△H2) | |
| B. | 用硅制作的太阳能电池是将化学能转化为电能 | |
| C. | 增加 Zn(g)的量,△H2变大 | |
| D. | Zn-Cu-CuSO4溶液构成的原电池中,Cu片质量增加,Zn片质量不变 |
20.下列对某些问题的认识正确的是( )
| A. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| B. | Na的金属性比Cu强,故可用Na与CuSO4溶液反应制取Cu | |
| C. | 不能用带玻璃塞的玻璃瓶盛放碱液 | |
| D. | 玻璃、水泥、陶瓷、水晶都是重要的硅酸盐材料 |
4.白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列化学键需要吸收的能量分别为:
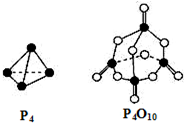
根据图所示的分子结构和有关数据计算该反应的△H,其中正确的是( )
| P-P | P-O | P=O | O=O | |
| 键能 (kJ/mol) | a | b | c | d |

根据图所示的分子结构和有关数据计算该反应的△H,其中正确的是( )
| A. | (4c+12b-6a-5d)kJ•mol-1 | B. | (6a+5d-4c-12b)kJ•mol-1 | ||
| C. | (4c+12b-4a-5d)kJ•mol-1 | D. | (4a+5d-4c-12b)kJ•mol-1 |
 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.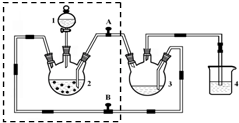 醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
醋酸亚铬水合物([Cr(CH3COO)2)]2•2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下: