题目内容
17.甲、乙两烧杯中各盛有100mL 3mol•L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为v(甲):V(乙)=2:3,则加入铝粉的质量为( )| A. | 4.05g | B. | 5.4 g | C. | 2.7g | D. | 8.1g |
分析 根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,应结束后测得生成的气体体积比为甲:乙=2:3,由化学反应方程式2Al+6H+═2Al3++3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,酸与金属反应时酸不过量,碱与金属反应时碱过量,以此来计算解答.
解答 解:盐酸和氢氧化钠溶液中溶质的物质的量均为0.1L×3mol/L=0.3mol,又两烧杯中分别加入等质最的铝粉,反应结束后测得生成的气体体积比为甲:乙=2:3,
设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,
则 2Al+6H+═2Al3++3H2↑
6 3
0.3mol x
解得x=0.15mol,
一定条件下,气体的物质的量之比等于体积之比,则碱与金属铝反应生成的氢气的物质的量为0.15mol×$\frac{3}{2}$=0.225mol,
碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,
则 2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.225mol
解得y=$\frac{2×0.225mol}{3}$=0.15mol,
则铝的质量为0.15mol×27g/mol=4.05g,
故选A.
点评 本题考查Al的化学性质及利用化学反应方程式的计算,把握铝与酸、碱反应水的化学反应方程式,酸碱足量、酸碱均不足量时得到的氢气的关系是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
7.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②盐酸 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸酸化的漂白粉溶液.
①氯气 ②盐酸 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸酸化的漂白粉溶液.
| A. | ③⑤ | B. | ③④⑤ | C. | ①②③ | D. | ①③④ |
8.下表是几种弱酸常温下的电离平衡常数:
(1)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看成酸,则酸性最强的是H3PO4,最弱的是HPO42-.
(2)多元弱酸的二级电离程度远小于一级电离的原因是一级电离产生的H+对二级电离有抑制作用.
(3)同浓度的CH3COO-、HCO3-、CO32-、S2-结合H+的能力由强到弱的顺序为S2->CO32->HCO3->CH3COO-.
(4)在温度相同时,各弱酸的K值不同,K值越大酸越强(填“强”或“弱”).
(5)根据K值大小判断下列反应能否发生:CH3COOH+H2PO4-不能(填“能”或“不能”,下同) H2CO3+HS-能.
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
(2)多元弱酸的二级电离程度远小于一级电离的原因是一级电离产生的H+对二级电离有抑制作用.
(3)同浓度的CH3COO-、HCO3-、CO32-、S2-结合H+的能力由强到弱的顺序为S2->CO32->HCO3->CH3COO-.
(4)在温度相同时,各弱酸的K值不同,K值越大酸越强(填“强”或“弱”).
(5)根据K值大小判断下列反应能否发生:CH3COOH+H2PO4-不能(填“能”或“不能”,下同) H2CO3+HS-能.
5.镁、铁、锌三种金属单质中的两种组成的混合物共12g,与足量的稀盐酸反应,产生标准状况下的氢气5.6L,由此可判断混合物中必定含有( )
| A. | Mg | B. | Fe | C. | Zn | D. | 无法判断 |
12.下列各项操作中,能发生“先沉淀后溶解”现象的是( )
①向BaCl2溶液中通入过量的SO2
②向Fe(OH)3胶体中逐滴滴入过量稀H2SO4
③向Na[Al(OH)4]溶液中逐滴加入过量的AlCl3溶液
④向澄清石灰水中通入过量的SO2
⑤向硅酸钠溶液中通入过量的CO2
⑥向AgNO3溶液中逐滴加入过量的氨水.
①向BaCl2溶液中通入过量的SO2
②向Fe(OH)3胶体中逐滴滴入过量稀H2SO4
③向Na[Al(OH)4]溶液中逐滴加入过量的AlCl3溶液
④向澄清石灰水中通入过量的SO2
⑤向硅酸钠溶液中通入过量的CO2
⑥向AgNO3溶液中逐滴加入过量的氨水.
| A. | ②④⑥ | B. | ①②④ | C. | ①③⑤⑥ | D. | ②③④⑤ |
2.能正确表示下列反应的离子方程式( )
| A. | 浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ | |
| C. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 金属铝溶于氢氧化钠溶液:2Al+2OH-+2H2O2[Al(OH)4]-+3H2↑ |
9.下列有关氧元素及其化合物的表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧原子的结构示意图: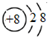 | |
| C. | 水分子的电子式: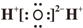 | |
| D. | 乙酸甲酯的结构简式HCOOC2H5 |
 高分子纳米活性钛无霸是钛氧化物经过光照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解存在生活空间中的一些有害物质(甲醛、氮氧化物等).
高分子纳米活性钛无霸是钛氧化物经过光照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解存在生活空间中的一些有害物质(甲醛、氮氧化物等).