题目内容
9.下列有关氧元素及其化合物的表示正确的是( )| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧原子的结构示意图: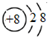 | |
| C. | 水分子的电子式: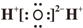 | |
| D. | 乙酸甲酯的结构简式HCOOC2H5 |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数,左下角为质子数;
B.氧原子的核电荷数=核外电子总数=8,最外层含有6个电子;
C.水分子为共价化合物,不存在阴阳离子;
D.HCOOC2H5为甲酸乙酯,乙酸甲酯为乙酸和甲醇生成的酯.
解答 解:A.质子数为8、中子数为10的氧原子的质量数为18,该原子可以表示为:${\;}_{8}^{18}$O,故A正确;
B.氧原子的最外层含有6个电子,其正确的原子结构示意图为: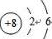 ,故B错误;
,故B错误;
C.水为共价化合物,其分子中含有2个O-H键,水的电子式为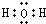 ,故C错误;
,故C错误;
D.乙酸甲酯是乙酸和甲醇发生酯化反应生成的酯,则乙酸甲酯的结构简式为:CH3COOCH3,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、原子结构示意图、元素符号、结构简式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
19.温州某地市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生反应生成I2,I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3稀溶液; c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位置是在步骤b后,增加操作:将分液漏斗充分振荡后静置.
(2)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加蒸馏水使其完全溶解,得1L溶液;
b.取100mL溶液,用稀硫酸酸化,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol•L-1的Na2S2O3溶液10.0mL,恰好反应完全.
根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)$\frac{12700}{3w}$mg/kg.
(3)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?否(填“是”或“否”),并说明理由KI3•H2O,在空气中容易被氧化,且加热碘易升华.
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+:在少是食盐样品溶液中滴加KSCN溶液,溶液呈无色,再加入氯水或双氧水,溶液呈血红色,则样品中有Fe2+.
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装时期 | |
| 分装企业 |
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3稀溶液; c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位置是在步骤b后,增加操作:将分液漏斗充分振荡后静置.
(2)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加蒸馏水使其完全溶解,得1L溶液;
b.取100mL溶液,用稀硫酸酸化,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol•L-1的Na2S2O3溶液10.0mL,恰好反应完全.
根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)$\frac{12700}{3w}$mg/kg.
(3)将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适?否(填“是”或“否”),并说明理由KI3•H2O,在空气中容易被氧化,且加热碘易升华.
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+:在少是食盐样品溶液中滴加KSCN溶液,溶液呈无色,再加入氯水或双氧水,溶液呈血红色,则样品中有Fe2+.
17.甲、乙两烧杯中各盛有100mL 3mol•L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为v(甲):V(乙)=2:3,则加入铝粉的质量为( )
| A. | 4.05g | B. | 5.4 g | C. | 2.7g | D. | 8.1g |
4.人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实的分析正确的是( )
| A. | 亚硝酸盐是还原剂 | B. | 维生素C是氧化剂 | ||
| C. | 维生素C将Fe3+还原为Fe2+ | D. | 亚硝酸盐被氧化 |
14.下列指定反应的离子方程式正确的是( )
| A. | 氨水吸收少量的CO2气体:NH3•H2O+CO2═NH4++HCO3- | |
| B. | Na2SO3溶液中SO32-的水解:SO32-+2H2O═H2SO3+2OH- | |
| C. | KClO3溶液与浓盐酸反应:ClO3-+5Cl-+6H+═3Cl2↑+3H2O | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH反应:Fe2++2OH-═Fe(OH)2↓ |
18.微电解法是利用原电池原理处理、净化高浓度有机废水的一种理想方法.在酸性、充入氧
气条件下的铁碳微电解法处理有机废水的过程中,有如下一些反应:
①O2+4H++4e-═2H2O
②O2+2H2O+4e-═4OH-
③4Fe2++O2+4H+═2H2O+4Fe3+
下列有关这种铁碳微电解法处理有机废水说法不合理的是( )
气条件下的铁碳微电解法处理有机废水的过程中,有如下一些反应:
①O2+4H++4e-═2H2O
②O2+2H2O+4e-═4OH-
③4Fe2++O2+4H+═2H2O+4Fe3+
下列有关这种铁碳微电解法处理有机废水说法不合理的是( )
| A. | 在处理废水的过程中,pH升高 | |
| B. | 铁做负极,电极反应式是 Fe-2e-═Fe2+ | |
| C. | 处理、净化过程中发生的反应都是氧化还原反应 | |
| D. | Fe(OH)3胶体,可净化除去废水中的悬浮物 |
19.800℃时,在2L密闭容器内充入0.50mol NO和0.25mol O2,发生如下反应:2NO(g)+O2(g)?2NO2(g)△H<0.体系中n( NO)随时间的变化如表:
(1)能说明该反应已达到平衡状态的是BCD
A.υ(NO2)正=υ(O2)逆 B.容器内压强保持不变
C.υ(NO)逆=2υ( O2)正 D.容器内气体颜色不变
(2)能使该反应的平衡向正反应方向移动的措施是BC
A.适当升高温度 B.缩小反应容器的体积
C.增大O2的浓度 D.选择高效催化剂.
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.50 | 0.35 | 0.28 | 0.25 | 0.25 | 0.25 |
A.υ(NO2)正=υ(O2)逆 B.容器内压强保持不变
C.υ(NO)逆=2υ( O2)正 D.容器内气体颜色不变
(2)能使该反应的平衡向正反应方向移动的措施是BC
A.适当升高温度 B.缩小反应容器的体积
C.增大O2的浓度 D.选择高效催化剂.
 已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D,C和F为同一主族元素,A与B、A与G形成共价化合物,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中离子半径最小的元素,F形成的化合物是造成酸雨的主要原因.请回答下列问题:
已知A、B、C、D、E、F、G是原子序数依次递增的短周期元素,已知A和D,C和F为同一主族元素,A与B、A与G形成共价化合物,B原子的最外层电子数比次外层多3,G元素的最高正化合价与最低负化合价的代数和为6,E是同周期中离子半径最小的元素,F形成的化合物是造成酸雨的主要原因.请回答下列问题: .画出G离子的结构示意图
.画出G离子的结构示意图 .
. 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.