题目内容
11.下列无色溶液中的离子能大量共存的是( )| A. | K+、Na+、MnO4-、SO42- | B. | OH-、K+、HCO3-、SO32- | ||
| C. | H+、Mg2+、Cl-、Br- | D. | Al3+、NH4+、OH-、NO3- |
分析 根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.MnO4-为紫色,与无色不符,故A错误;
B.OH-、HCO3-结合生成水和碳酸根离子,不能共存,故B错误;
C.该组离子之间不反应可大量共存,故C正确;
D.Al3+、NH4+均与OH-结合发生反应,不能共存,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
1.草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向10mL 0.01mol/L NaHC2O4溶液中滴加0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A. | V(NaOH)=0时,c(H+)=1×10-2 mol/L | |
| B. | V(NaOH)=10mL时,c(H+)=1×10-7 mol/L | |
| C. | V(NaOH)<10mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) | |
| D. | V(NaOH)>10mL时,c(C2O42-)>c(Na+)>c(HC2O4-) |
2.下面不能由单质直接化合而得到的化合物( )
| A. | FeCl2 | B. | AlCl3 | C. | FeS | D. | Fe3O4 |
19.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | Cl2 | B. | BaSO4 | C. | SO2 | D. | CH3COOH |
6. 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
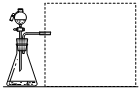
Ⅱ.实验设计(1)【方案一】测量气体产物:在相同温度下,利用右图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).
上图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据
分别是5.0、25.
Ⅲ.讨论与交流:(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式
酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象
是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计(1)【方案一】测量气体产物:在相同温度下,利用右图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).
上图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据
| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | 25 | ① | 2.0 | 4.0 | 4.0 | t2 |
| 3 | ② | 7.0 | 2.0 | 4.0 | 2.0 | t3 |
Ⅲ.讨论与交流:(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式
酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象
是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
3.琥珀酸与乙醇反应生成琥珀酸二乙酯(结构如图所示),下列有关说法正确的是( )
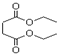

| A. | 1mol琥珀酸二乙酯能与4mol的NaOH反应 | |
| B. | 琥珀酸二乙酯在一定条件下能发生取代、加成和氧化反应 | |
| C. | 琥珀酸的分子式为C4H8O4 | |
| D. | 琥珀酸分子中含有六元环 |
20.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 78 g Na2O2中存在的共价键总数为NA | |
| B. | 0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 氢氧燃料电池负极消耗2.24 L气体时,电路中转移的电子数为0.1NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
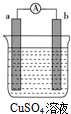 某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题:
某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题: