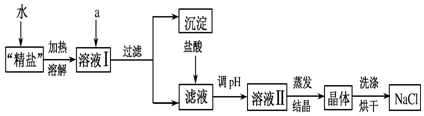
��Ŀ����
17���⻯�ƣ�CaH2��������һ�ִ�����ϣ��ǵ�ɽ�˶�Ա���õ���Դ�ṩ����ij��ѧС���ͬѧ����ʦ��ָ�����Ʊ��⻯�ƣ����������ϡ�
����Ca�IJ���������
�ٳ��»����������Ca������������Ӧ��
��Ca������ˮ�����������ҷ�Ӧ�����������ƺ����������ų��������ȣ�
��Ca+H2 $\frac{\underline{\;\;��\;\;}}{\;}$ CaH2�����壩
����CaH2�IJ���������
�ٳ��£�CaH2+2H2O=Ca��OH��2+2H2���� ��CaH2Ҫ�ܷⱣ�森
������ʵ�顿
��С��ͬѧ��Ƶ���ȡװ����ͼ��ʾ���̶�װ���ԣ���

�ش��������⣺
��1��д��Ca������ˮ������Ӧ�Ļ�ѧ����ʽ��Ca+2H2O=Ca��OH��2+H2����
��2��B��D����ʢ�Լ���ͬ�����Լ�ΪŨ���ᣨ�����ƣ���D�и��Լ��������Ƿ�ֹ�����е�ˮ��������C�У�
��3��ʵ��ʱ�ȴ�A�л�����һ��ʱ����ٵ�ȼC�оƾ��ƣ���Ŀ���ǣ��ų�װ���ڵĿ�������ֹ����ʱ������ը��
��ʵ�鷴˼��
��С��ͬѧͨ����˼������⣺�����Ƶõ�CaH2�Ƿ���
�����ٴ����ʵ����м��飬ʵ�鲽�����£�
����1�����װ�������ԣ�װ��������ˮ���ѳƺ�����Ϊm g��CaH2��Ʒ����ͼ��ʾ�����������̶�װ���ԣ���

����2����Y�ι���б��ʹA�е�ˮȫ������B�У���Ʒȫ����Ӧ����ȴ�����£���ȡ��Ͳ����ΪV mL��
��4������ʵ�������µ�����Ħ�����ΪVm L/mol����V=$\frac{1000mV{\;}_{m}}{21}$mLʱ����m��Vm��ʾ���������Ƶõ�CaH2��Ʒ�Ǵ����ģ�
���� ��1��Ca������ˮ������Ӧ�����������ƺ�������
��2��������Ϣ����������Ʒ�Ӧ�����Ǹ�����������⻯�Ʋ�����ˮ�Ӵ������DҲ�Ǹ���װ�ã�
��3�����������Ŀ�ȼ�Է�����
��ʵ�鷴˼������ͼʾ��Ҫ��֤�⻯���Ƿ�����ȡһ�����⻯����Ʒ��ˮ��ȫ��Ӧ������������������������⻯�Ƶ�������Ȼ������Ʒ�����Ƚϣ���������Ʒ������Ϊ������
��� �⣺��1��Ca������ˮ������Ӧ�����������ƺ���������ѧ����ʽCa+2H2O=Ca��OH��2+H2����
�ʴ�Ϊ��Ca+2H2O=Ca��OH��2+H2����
��2����������Ƽ����Ƶ��⻯�ƣ������ˮ�����������ҷ�Ӧ�����������ƺ����������ų��������ȣ�������Ʒ�Ӧ�����������Ǹ��������������ȡ��������ͨ��Ũ������и�������ɵ��⻯����ˮ��Ӧ�����������ƺ����������Ϊ��ֹ��ֹ�����е�ˮ��������C�У�����D��װ��Ũ������и��
�ʴ�Ϊ��Ũ�����ֹ�����е�ˮ��������C�У�
��3����ȼ�������������ܻᷢ����ը�����������Ƽ��ȷ�Ӧǰ�轫װ���ڵĿ����ų�����ʵ��ʱ�ȴ�A�л�����һ��ʱ����ٵ�ȼC�оƾ��ƣ����ų�װ���ڵĿ�������ֹ����ʱ������ը��
�ʴ�Ϊ���ų�װ���ڵĿ�������ֹ����ʱ������ը��
��4��ͨ������ʵ��ɷ������Ƶõ��⻯���Ƿ����������ǣ�����ʵ��ó����������������⻯����ˮ��Ӧ�Ļ�ѧ����ʽ������������⻯�Ƶ������������⻯����Ʒ�������Աȣ���������Ʒ������Ϊ������������
CaH2+2H2O=Ca��OH��2+2H2��
42 2
m $\frac{V��10{\;}^{-3}L}{V{\;}_{m}L/mol}$
�� $\frac{42}{m}$=$\frac{2}{\frac{V��10{\;}^{-3}}{V{\;}_{m}}}$��V=$\frac{1000mV{\;}_{m}}{21}$���ʴ�Ϊ��$\frac{1000mV{\;}_{m}}{21}$��
���� ���⿼�����ʵ��Ʊ�ʵ�鷽����Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ��ʵ��װ�õ����ü�ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬�ۺ��Խ�ǿ����Ŀ�ѶȲ���

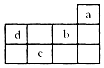
| A�� | aԭ��������Ӳ��ϵĵ�����Ϊ8 | |
| B�� | b������������Ӧˮ����Ϊǿ�� | |
| C�� | c���ڵ����ֳ��������������������һ����ԭ�� | |
| D�� | d��b���ǵڶ����ڵķǽ���Ԫ�أ���d��b�ķǽ�����ǿ |
| A�� | CO2+H2O=H2CO3 | B�� | CaCO3$\frac{\underline{\;����\;}}{\;}$CO2��+CaO | ||
| C�� | CaCO3+2HCl=CaCl2+H2O+CO2�� | D�� | 2Na+Cl2$\frac{\underline{\;��ȼ\;}}{\;}$NaCl |
| A�� | ��������Һ��c��H+���ֱ�Ϊa1 mol•L-1��a2 mol•L-1��a3 mol•L-1�������ǵĴ�С��ϵΪ$\frac{1}{2}$a2=a1=a3 | |
| B�� | �����������������ֱ��������NaOH��Һ��Ӧ�������ɵ��ε����ʵ�������Ϊb1 mol��b2 mol��b3 mol�������ǵĴ�С��ϵΪb1=b2��b3 | |
| C�� | �ֱ��������������к�һ������NaOH��Һ�������Σ�����Ҫ�������ֱ�ΪV1��V2��V3�����С��ϵΪV1=V2=V3 | |
| D�� | �ֱ���Zn��Ӧ����ʼʱ����H2�����ʷֱ�Ϊv1��v2��v3�����С��ϵΪv2��v1��v3 |
 �������Ͼ���Ԫ�ط��ű�ʾ��
�������Ͼ���Ԫ�ط��ű�ʾ��