题目内容
20.为了配制100mL1mol/LNaOH溶液,其中有下列几个操作:①NaOH用纸盛载称量 ②选刚用蒸馏水洗净的100mL容量瓶进行配制 ③NaOH在烧杯里刚好完全溶解,即把溶液移入容量瓶 ④用蒸馏水洗涤烧杯内壁两次,洗涤液都移入容量瓶;其中操作错误的是( )| A. | ① | B. | ② | C. | ③ | D. | ④ |
分析 ①NaOH固体易潮解,具有腐蚀性;
②配制一定物质的量浓度溶液应在容量瓶中进行,依据配制溶液体积选择容量瓶规格,容量瓶定容时还需要加入蒸馏水;
③容量瓶为精密仪器,不能盛放过热、过冷液体;
④为保证实验成功,应将溶质全部转移到容量瓶.
解答 解:①NaOH固体易潮解,具有腐蚀性,应放在烧杯进行称量,故错误;
②配制100mL1mol/LNaOH溶液,应选择100mL容量瓶,容量瓶定容时还需要加入蒸馏水,所以使用前不需要干燥,故正确;
③氢氧化钠溶解产生大量的热,不能立即移入容量瓶,故错误;
④为保证实验成功,应将溶质全部转移到容量瓶,所以用蒸馏水洗涤烧杯内壁两次,洗涤液都移入容量瓶,故正确;
故选:AC.
点评 本题主要考查了配制一定物质的量的溶液的配制方法和注意事项,难度不大,注意易潮解、具有腐蚀性的药品应在玻璃器皿中迅速称量,注意容量瓶使用方法和注意事项.

练习册系列答案
相关题目
5.氨催化氧化法制硝酸的原理为4NH3(g)+5O2(g)$?_{△}^{Pt}$4NO(g)+6H2O(g).在浓氨水中通入空气,将赤热铂
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
| A. | 上述反应在较高温度下才能自发进行 | |
| B. | 该反应的正反应活化能小于逆反应活化能 | |
| C. | 该反应中,断裂化学键的总键能大于形成化学键的总键能 | |
| D. | 若NH3和O2的混合气发生上述反应,气体通入足量水中,剩余气体一定是O2 |
12.下列物质间的反应不属于离子反应的是( )
| A. | CO+O2 | B. | NaCl+AgNO3 | C. | CaCO3+HCl | D. | CuO+H2 |
9.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p1;②1s22s22p63s23p3;③1s22s22p5.则下列有关比较中正确的是( )
| A. | 第一电离能:③>②>① | B. | 原子半径:③>②>① | ||
| C. | 电负性:③<②<① | D. | 最高正化合价:③>②>① |
10.下列叙述正确的是( )
| A. | 0.012kg碳所含的碳原子数就是阿伏加德罗常数 | |
| B. | 阿伏加德罗常数没有单位 | |
| C. | 阿伏加德罗常数通常用NA表示,6.02×1023称为阿伏加德罗常数 | |
| D. | 阿伏加德罗常数个粒子的集体就是1mol |
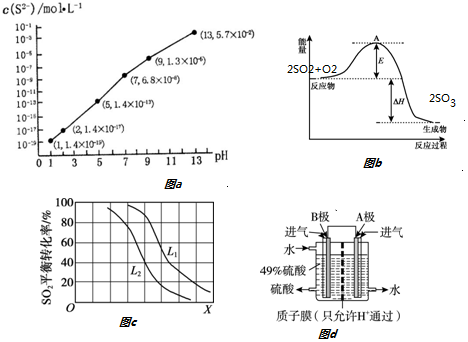
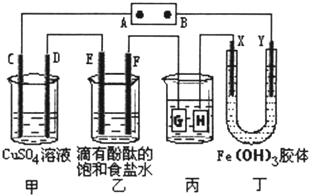 如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深.请回答:
如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深.请回答: