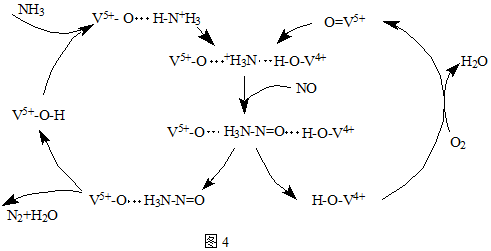
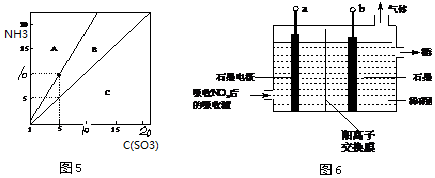
��Ŀ����
10����Ԫ���ж��ֻ��ϼۣ����γɶ��ֻ���� H2S��SO2�ڹ�ũҵ�����о�����ҪӦ�ã���1��H2S��������ˮ�γɵ���������һ�ֶ�Ԫ���ᣬ25��ʱ����0.10mol/L H2S��Һ�У�ͨ��HCl��������NaOH�����Ե�����ҺpH����ҺpH��c��S2-����ϵ��ͼa��ʾ��������Һ����ı仯��H2S�Ļӷ�����
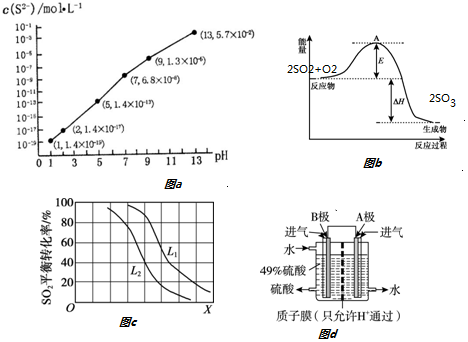
��pH=13ʱ����Һ�е�c��H2S��+c��HS-��=0.043mol/L��
��ij��Һ��0.010mol/LFe2+��δ֪Ũ�ȵ�Mn2+��0.10mol/L H2S������ҺpH=2ʱ��Fe2+��ʼ��������Mn2+��ʼ����ʱ����Һ��$\frac{c��M{n}^{2+}��}{c��F{e}^{2+}��}$=2��106��
��֪��Ksp��FeS��=1.4��10-19��Ksp��MnS��=2.8��10-13��
��2�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮��֪��SO2��g��+$\frac{1}{2}$O2��g��?SO3��g����H=-99kJ/mol��ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=$\frac{10}{3}$����Ӧ���̵������仯��ͼb��ʾ��
��ͼb�С�H=-198kJ/mol���÷�Ӧͨ����V2O5����������V2O5��ʹͼb��A�㽵�ͣ���������Ϊ�����ı��˷�Ӧ���̣�ʹ���E���ͣ�
�ڸ��¶��£���100L�ĺ����ܱ������У�����3.0mol SO2��g����16.0mol O2��g����3.0mol SO3��g������Ӧ��ʼʱv�������� v���棩�����������������=������
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȣ�ͼc��ʾLһ��ʱ��SO2��g����ƽ��ת������X�ı仯��ϵ����X���������������¶ȣ�L1��L2�Ĵ�С��ϵΪL1��L2��������2SO2+O2 $\frac{\underline{\;����\;}}{\;}$2SO3��Ӧ�ġ�H=-198kJ/mol���Ƿ��ȷ�Ӧ����ѹǿһ��ʱ���¶����ߣ�ƽ�����ƣ�SO2ƽ��ת���ʼ�С��
��3���ҹ��ĿƼ���ԱΪ������SO2����Ⱦ������ԭ���ԭ�������Ϊ���������SO2��O2���Ʊ����ᣬ���װ����ͼd��ʾ���缫A��BΪ��IJ��ϣ�
��A�������������������������
��B���ĵ缫��Ӧʽ��SO2+2H2O-2e-�TSO42-+4H+��
���� ��1����pH=13ʱ��c��S2-��=5.7��10-2mol/L����0.10mol•L-1H2S��Һ�и������غ�c��H2S��+c��HS-��+c��S2-��=0.10mol•L-1��
�ڵ�Qc=Ksp��MnS��ʱ��ʼ�������ɴ���������ӵ�Ũ�ȣ����ͼ��ó���ʱ��pH������MnS��FeS��Ksp���㣻
��2����ͼ�������Ӧ�ʱ���2mol����������ȫ��Ӧ����������EΪ��ܣ���ܵĴ�С�뷴Ӧ���أ���������ܽ��ͷ�Ӧ�Ļ�ܣ�
�ڼ����ʱ��Ӧ��Ũ����Q����ƽ�ⳣ���Ƚ��жϷ�Ӧ���еķ���
�۸÷�ӦΪ���������С�ķ�Ӧ���������ѹǿ��ת���ʴ�Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У���������ת���ʼ�С���ݴ��жϣ�
��3���ٸ�ԭ����У�������ʧ���ӱ����������Ը�����Ͷ�ŵ������Ƕ�������������ʧ���Ӻ�ˮ��Ӧ������������Ӻ������ӣ�������Ͷ�ŵ������������������������õ��Ӻ������ӷ�Ӧ����ˮ�����������ˮ�ij��ڷ���֪��B���Ǹ�����A����������
��B���ϵĵ缫��Ӧ��������ʧ���Ӻ�ˮ��Ӧ������������Ӻ������ӣ�
��� �⣺��1���ٸ�����ҺpH��c��S2-����ϵͼpH=13ʱ��c��S2-��=5.7��10-2mol/L����0.10mol•L-1H2S��Һ�и������غ�c��H2S��+c��HS-��+c��S2-��=0.10mol•L-1������c��H2S��+c��HS-��=0.1-5.7��10-2=0.043mol/L��
�ʴ�Ϊ��0.043��
�ڵ�Qc=Ksp��FeS��ʱ��ʼ����������c��S2-��=$\frac{Ksp��FeS��}{c��F{e}^{2+}��}$=$\frac{1.4��1{0}^{-19}}{0.01}$mol/L=1.4��10-17mol/L�����ͼ��ó���ʱ��pH=2������pH=2ʱ�������ӿ�ʼ������
��Һ��$\frac{c��M{n}^{2+}��}{c��F{e}^{2+}��}$=$\frac{Ksp��MnS��}{Ksp��FeS��}$=$\frac{2.8��1{0}^{-13}}{1.4��1{0}^{-19}}$mol/L=2��106��
�ʴ�Ϊ��2��2��106��
��2��SO2��g��+$\frac{1}{2}$O2��g��?SO3��g����H=-99kJ/mol��
��ͼ�������֪2molSO2������ȫ����Ӧ����Ӧ�ʱ��H=-99kJ/mol��2mol=-198KJ��EΪ��ܣ���Ӧ�ȿɱ�ʾΪA��C��ܵĴ�С֮���ܵĴ�С�뷴Ӧ���أ���������ı��˷�Ӧ��;�������ͷ�Ӧ����Ļ�ܣ�����E�ı仯�Ǽ�С��
�ʴ�Ϊ��-198����Ϊ�����ı��˷�Ӧ������ʹ���E���ͣ�
�ڸ��¶��£���100L�ĺ����ܱ������У�����3.0mol SO2��g����16.0mol O2��g����3.0mol SO3��g����Ũ����Qc=$\frac{\frac{3.0mol}{100L}}{\frac{3.0mol}{100L}����\frac{16.0mol}{100}��^{\frac{1}{2}}}$=2.5��K=$\frac{10}{3}$��
��Ӧ��ʼʱ��������v���棩
�ʴ�Ϊ������
����ͼ��֪��XԽ��ת����Խ�ͣ��÷�Ӧ����ӦΪ���������С�ķ�Ӧ���������ѹǿ��������̼��ת���ʴ�����X��ʾ�¶ȣ��¶����ߣ�ת�����½���ƽ�������ƶ�������ѹǿ��ת���ʴ�����L1��L2��
�ʴ�Ϊ���¶ȣ�L1��L2��2SO2+O2$\frac{\underline{\;����\;}}{\;}$2SO3��Ӧ�ġ�H=-198 kJ/mol���Ƿ��ȷ�Ӧ����ѹǿһ��ʱ���¶����ߣ�ƽ�����ƣ�SO2ƽ��ת���ʼ�С��
��3���ٸ�ԭ����У�������ʧ���ӱ����������Ը�����Ͷ�ŵ������Ƕ�������������ʧ���Ӻ�ˮ��Ӧ������������Ӻ������ӣ�������Ͷ�ŵ������������������������õ��Ӻ������ӷ�Ӧ����ˮ�����������ˮ�ij��ڷ���֪��B���Ǹ�����A����������
�ʴ�Ϊ��������
�ڷ�����֪B���ϵĵ缫��ӦʽΪ��SO2-2e-+2H2O�TSO42-+4H+��
�ʴ�Ϊ��SO2-2e-+2H2O�TSO42-+4H+��
���� ���⿼�黯ѧƽ�ⳣ����ƽ��״̬���жϡ�ȼ�ϵ�ء�������ԭ��Ӧ���ζ������֪ʶ���漰�������ϴ���Ŀ�Ѷ��еȣ�

 Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�| A�� | ��˾ƥ������֪�Ľ�����ʹ��ҩ���ѧ��Ϊˮ���� | |
| B�� | ���ڵĴ���ʹ�ð�˾ƥ�ֻ����ˮ�����ж���Ӧͣҩ����ע��Na2CO3��Һ | |
| C�� | ��ù������Ҫ�Ŀ����أ�����һ������������ | |
| D�� | ��Ʒ��ָ��ҽ��Ŀ�Ķ�����ʹ�ò��������Ե�ҩƷ |
| A�� | Cl2+NaBr | B�� | Br2+KI | C�� | Br2+KCl | D�� | Cl2+KI |
| A�� | ���¶��£���Ӧ��ƽ�ⳣ����$\frac{1}{64}$ | |
| B�� | 0��2min�ڣ�HI��ƽ����Ӧ����Ϊ0.1mol•L-1•min-1 | |
| C�� | �ں��������£������ϵ�г���HI���壬ƽ�ⲻ�ƶ�����Ӧ���ʲ��� | |
| D�� | �����¶ȣ�ƽ��������Ӧ�����ƶ���ֻ������Ӧ���ʼӿ� |
| A�� | ��ֹ����й����ӡ�����Ǧ���ؽ���Ԫ�ض�������ˮԴ����Ⱦ | |
| B�� | �������е�ʯī�缫 | |
| C�� | ��ʹ�����й�ĵ��Һ��ʴ������Ʒ | |
| D�� | �������еĸ��ֽ��������ϰ�װ�� |
��C4H10��g��+$\frac{13}{2}$O2��g���T4CO2��g��+5H2O��l����H=-2 878kJ•mol-1
��C4H10��g��+$\frac{13}{2}$O2��g���T4CO2��g��+5H2O��g����H=-2 658kJ•mol-1
��C4H10��g��+$\frac{9}{2}$O2��g���T4CO��g��+5H2O��l����H=-1 746kJ•mol-1
��C4H10��g��+$\frac{9}{2}$O2��g���T4CO��g��+5H2O��g����H=-1 526kJ•mol-1
�ɴ��жϣ��������ȼ������ ��������
| A�� | ��H=-2 878 kJ•mol-1 | B�� | ��H=-2 658 kJ•mol-1 | ||
| C�� | ��H=-1 746 kJ•mol-1 | D�� | ��H=-1 526 kJ•mol-1 |