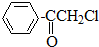题目内容
已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10;C原子的最外层电子数是核外电子总数的
;D与C同一主族,E-比C2-多一个电子层.试回答:
(1)D与E两元素相比较,非金属性较强的是 (填元素名称),请你自选试剂设计实验验证该结论(说明试剂、简单操作、实验现象)
(2)A、C、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 ;
(3)B和C形成的一种化合物是参与大气循环的气体,写出它的电子式 .
| 3 |
| 4 |
(1)D与E两元素相比较,非金属性较强的是
(2)A、C、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(3)B和C形成的一种化合物是参与大气循环的气体,写出它的电子式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10,分子中5个原子的平均电子数为2,故A为H元素、B为碳元素;D与C同一主族,则C处于第二周期、D处于第三周期,C原子的最外层电子数是核外电子总数的
,令C的最外层电子数为x,则
×(2+x)=x,解得x=6,则C为氧元素、D为硫元素;E-比C2-多一个电子层,则E为Cl元素,据此解答.
| 3 |
| 4 |
| 3 |
| 4 |
解答:
解:A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10,分子中5个原子的平均电子数为2,故A为H元素、B为碳元素;D与C同一主族,则C处于第二周期、D处于第三周期,C原子的最外层电子数是核外电子总数的
,令C的最外层电子数为x,则
×(2+x)=x,解得x=6,则C为氧元素、D为硫元素;E-比C2-多一个电子层,则E为Cl元素,
(1)同周期自左而右非金属性增强,故非金属性Cl>S;将Cl2 通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强,
故答案为:氯;将Cl2 通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强;
(2)H、O、S间可形成甲、乙两种微粒,它们均为负一价的双原子阴离子且甲有18个电子,乙有10个电子,则甲是HS-、乙是OH-,则甲与乙反应为S 2-和H2O,该反应的离子方程式为 HS-+OH-=S 2-+H2O,
故答案为:HS-+OH-=S 2-+H2O;
(3)B和C形成的一种化合物是参与大气循环的气体,则该气体是CO2,CO2的电子式为 ,
,
故答案为: .
.
| 3 |
| 4 |
| 3 |
| 4 |
(1)同周期自左而右非金属性增强,故非金属性Cl>S;将Cl2 通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强,
故答案为:氯;将Cl2 通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强;
(2)H、O、S间可形成甲、乙两种微粒,它们均为负一价的双原子阴离子且甲有18个电子,乙有10个电子,则甲是HS-、乙是OH-,则甲与乙反应为S 2-和H2O,该反应的离子方程式为 HS-+OH-=S 2-+H2O,
故答案为:HS-+OH-=S 2-+H2O;
(3)B和C形成的一种化合物是参与大气循环的气体,则该气体是CO2,CO2的电子式为
 ,
,故答案为:
 .
.
点评:本题考查位置结构性质的相互关系及应用,涉及电子式、非金属性强弱的判断等知识点,注意掌握常见10电子、18电子的微粒,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
“在3支大小相同的试管中各加入2mL 5%的H2O2溶液,再向其中2支试管中分别加入少量MnO2粉末、2滴1mol/LFeCl3溶液.对比观察现象.”该实验的目的是( )
| A、探究浓度对反应速率的影响 |
| B、探究温度对反应速率的影响 |
| C、探究固体表面积对反应速率的影响 |
| D、探究催化剂对反应速率的影响 |
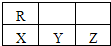 如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )| A、R的气态氢化物与它的含氧酸之间能发生化学反应 |
| B、原子半径大小顺序是:Z>Y>X |
| C、Y、Z的单质在一定条件下均能与Fe反应 |
| D、X、Y、Z中Z的氧化物对应的水化物的酸性最强 |
 水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图象,模型如图所示,下列关于水的说法正确的是( )
水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图象,模型如图所示,下列关于水的说法正确的是( )| A、水是弱电解质 |
| B、可燃冰是可以燃烧的水 |
| C、氢氧两种元素只能组成水 |
| D、0℃时冰的密度比液态水的密度大 |
 X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子.
X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子.