题目内容
A、B、C、D、E、F都是短周期元素,原子序数依次增大,B、C、D同周期,A、E同主族.A、C能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1.B元素原子有两个未成对电子,D是周期表中电负性最大的元素,F是地壳中含量最多的金属元素.根据以上信息回答下列问题:
(1)写出A、C、E三种元素的符号:
A ,C ,E .
(2)甲、乙两分子中含有非极性共价键的是 (填分子式),它的电子式为 .
(3)C、D、F的离子中,半径最小的是 (填离子符号)
(4)用氢键表示式写出液态D的氢化物中存在的氢键 .
(1)写出A、C、E三种元素的符号:
A
(2)甲、乙两分子中含有非极性共价键的是
(3)C、D、F的离子中,半径最小的是
(4)用氢键表示式写出液态D的氢化物中存在的氢键
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E、F都是短周期元素,原子序数依次增大,A、C能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1,形成的化合物是水和双氧水,则A是H元素,C是O元素;D是周期表中电负性最大的元素,所以D是F元素;F是地壳中含量最多的金属元素,则F是Al元素;B、C、D同周期,处于第二周期,B元素基态原子有两个未成对电子,原子序数小于O元素,故其核外电子排布为1s22s22p2,则B是C元素,C的原子序数介于碳、氧之间,则C是N元素,A、E同主族,E的原子序数大于氧,则E是Na元素,据此解答.
解答:
解:A、B、C、D、E、F都是短周期元素,原子序数依次增大,A、C能形成两种液态化合物甲和乙,原子个数比分别为2:1和1:1,形成的化合物是水和双氧水,则A是H元素,C是O元素;D是周期表中电负性最大的元素,所以D是F元素;F是地壳中含量最多的金属元素,则F是Al元素;B、C、D同周期,处于第二周期,B元素基态原子有两个未成对电子,原子序数小于O元素,故其核外电子排布为1s22s22p2,则B是C元素,C的原子序数介于碳、氧之间,则C是N元素,A、E同主族,E的原子序数大于氧,则E是Na元素,
(1)由上述分析可知,A为H元素、C为N元素、E为Na元素,故答案为:H;N;Na;
(2)通过以上分析知,甲是H2O,乙是H2O2,H2O2分子中氧原子和氧原子之间存在非极性共价键,双氧水分子的电子式为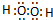 ,
,
故答案为:H2O2;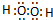 ;
;
(3)N3-、F-、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故半径最小的是Al3+,故答案为:Al3+;
(4)液态D的氢化物为HF,存在的氢键为H-F…H-F,故答案为:H-F…H-F.
(1)由上述分析可知,A为H元素、C为N元素、E为Na元素,故答案为:H;N;Na;
(2)通过以上分析知,甲是H2O,乙是H2O2,H2O2分子中氧原子和氧原子之间存在非极性共价键,双氧水分子的电子式为
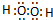 ,
,故答案为:H2O2;
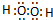 ;
;(3)N3-、F-、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故半径最小的是Al3+,故答案为:Al3+;
(4)液态D的氢化物为HF,存在的氢键为H-F…H-F,故答案为:H-F…H-F.
点评:本题考查位置结构性质的关系及应用,明确元素的推断是解答本题的关键,侧重对常用化学用语考查,注意掌握氢键的表示,难度中等.

练习册系列答案
相关题目
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的是( )
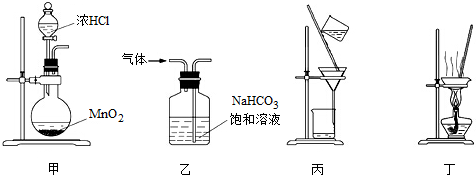

| A、用装置甲制取氯气 |
| B、用装置乙除去氯气中混有的少量氯化氢 |
| C、用装置丙分离二氧化锰和氯化锰溶液 |
| D、用装置丁蒸干氯化锰溶液制MnCl2?4H2O |

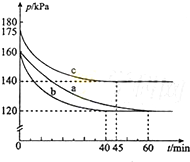 化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题;
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题;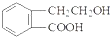 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.