题目内容
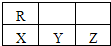 如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )| A、R的气态氢化物与它的含氧酸之间能发生化学反应 |
| B、原子半径大小顺序是:Z>Y>X |
| C、Y、Z的单质在一定条件下均能与Fe反应 |
| D、X、Y、Z中Z的氧化物对应的水化物的酸性最强 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X原子最外层电子数比次外层电子数少3,推知X为P,则R、Y、Z依次为N、S、Cl,根据元素周期律的递变规律判断元素的非金属性、原子半径以及对应化合物的性质.
解答:
解:X原子最外层电子数比次外层电子数少3,推知X为P,则R、Y、Z依次为N、S、Cl,则
A.R的气态氢化物为氨气,能与它的含氧酸之间能发生化学反应生成铵盐,故A正确;
B.同周期,从左向右原子半价减小,则原子半径大小顺序是X>Y>Z,故B错误;
C.Y、Z的单质在一定条件下均能与Fe反应,分别生成FeS、FeCl3,故C正确;
D.X、Y、Z的非金属性增强,对于的最高价氧化物的水化物酸性增强,则Z的最高价氧化物对应的水化物的酸性最强,故D错误;
故选AC.
A.R的气态氢化物为氨气,能与它的含氧酸之间能发生化学反应生成铵盐,故A正确;
B.同周期,从左向右原子半价减小,则原子半径大小顺序是X>Y>Z,故B错误;
C.Y、Z的单质在一定条件下均能与Fe反应,分别生成FeS、FeCl3,故C正确;
D.X、Y、Z的非金属性增强,对于的最高价氧化物的水化物酸性增强,则Z的最高价氧化物对应的水化物的酸性最强,故D错误;
故选AC.
点评:本题考查位置结构性质的相互关系应用,题目难度中等,注意周期律的递变规律,本题易错点为D,注意非金属性与最高价含氧酸酸性的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质会造成“白色污染”的是( )
| A、白纸 | B、石灰 |
| C、废弃塑料 | D、蛋白质 |
 2012年3月上海新闻栏目曾报道杭州世纪联华超市在售的某品牌鸡蛋为“橡皮弹”,煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋.专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致.结构简式如图所示:下列说法不正确的是( )
2012年3月上海新闻栏目曾报道杭州世纪联华超市在售的某品牌鸡蛋为“橡皮弹”,煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋.专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致.结构简式如图所示:下列说法不正确的是( )| A、该化合物的分子式为:C30H30O8 |
| B、1mol棉酚最多可与14mol H2加成,与6mol NaOH反应 |
| C、该物质可以与碳酸钠溶液反应 |
| D、该物质可以使酸性高锰酸钾溶液褪色 |
某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其它均为Cu,则( )


| A、电流方向:电极Ⅳ→A→电极Ⅰ |
| B、电极Ⅰ发生还原反应 |
| C、电极Ⅱ逐渐溶解 |
| D、电极Ⅲ的电极反应:Cu2++2e-═Cu |
化学与生活密切相关.下列说法不正确的是( )
| A、乙烯可作水果的催熟剂 |
| B、硅胶可作袋装食品的干燥剂 |
| C、福尔马林可作食品的保鲜剂 |
| D、氢氧化铝可作胃酸的中和剂 |
