题目内容
20.下列反应中,属于氧化还原反应的是( )| A. | CaCO3+2HCl═CaCl2+CO2↑+H2O | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 2Na2O2+2CO2═2Na2CO3+O2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
分析 属于氧化还原反应,说明该反应中有电子转移,其特征是有元素化合价升降,据此分析解答.
解答 解:A.元素化合价没有发生变化,为复分解反应,故A不选;
B.元素化合价没有发生变化,为化合反应,不是氧化还原反应,故B不选;
C.O元素化合价发生变化,属于氧化还原反应,故C选;
D.元素化合价没有发生变化,不是氧化还原反应,故D不选.
故选C.
点评 本题考查了氧化还原反应判断,根据元素化合价变化来分析解答即可,知道常见元素化合价及常见反应类型,题目难度不大.

练习册系列答案
相关题目
11.下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
| A. | 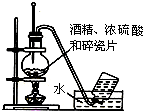 实验室用乙醇制取乙烯 | B. | 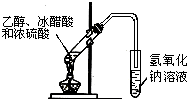 实验室制取乙酸乙酯 | ||
| C. |  分离苯和甲苯 | D. |  实验室制取硝基苯 |
5.下列实验操作中错误的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 过滤操作时,应用玻璃棒作引流 |
12.如图所示,6个编号分别代表下列物质中的一种物质,凡是直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )
a.Al b.Fe2O3 c.NaOH 溶液 d.Cl2 e.NH3 f.氢碘酸溶液.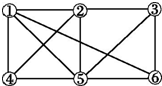
a.Al b.Fe2O3 c.NaOH 溶液 d.Cl2 e.NH3 f.氢碘酸溶液.

| A. | a 或b | B. | c | C. | d 或e | D. | f |
9.下列性质比较中不正确的是( )
| A. | 沸点:CBr4>CF4 | B. | 水溶性:HBr>Br2 | ||
| C. | 硬度:镁>镁铝合金 | D. | 熔点:金刚石>NaCl |
10.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 7.8g苯中碳碳双键的数目为0.3NA | |
| B. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的个数为NA | |
| C. | 常温常压,11.2L NO和O2混合气体的原子数为NA | |
| D. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数为0.46NA |
 一定温度下,在密闭容器内进行某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示.
一定温度下,在密闭容器内进行某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图所示.
 .
.