题目内容
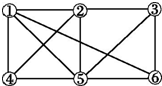
12.如图所示,6个编号分别代表下列物质中的一种物质,凡是直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁).图中⑤表示的物质是( )a.Al b.Fe2O3 c.NaOH 溶液 d.Cl2 e.NH3 f.氢碘酸溶液.
| A. | a 或b | B. | c | C. | d 或e | D. | f |
分析 编号⑤和其他5种物质都能发生反应,因此只能是氢碘酸,发生反应的化学方程式依次为:2Al+6HI═2AlI3+3H2↑;Fe2O3+6HI═2FeI2+I2+3H2O;NaOH+HI═NaI+H2O;HI+NH3═NH4I;Cl2+2HI═I2+2HCl.
解答 解:编号⑤和其他5种物质都能发生反应,因此只能是氢碘酸,发生反应的化学方程式依次为:2Al+6HI═2AlI3+3H2↑;Fe2O3+6HI═2FeI2+I2+3H2O;NaOH+HI═NaI+H2O;HI+NH3═NH4I;Cl2+2HI═I2+2HCl,故选:D.
点评 本题考查无机物推断,关键是熟练掌握元素化合物性质,注意对基础知识的理解掌握.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
3.NaCl是一种化工原料,可以制备一系列物质(如下图).下列说法正确的是( )
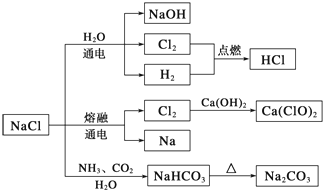

| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 电解NaCl溶液的阳极产物为H2和NaOH | |
| D. | 图中所示转化反应都是氧化还原反应 |
20.下列反应中,属于氧化还原反应的是( )
| A. | CaCO3+2HCl═CaCl2+CO2↑+H2O | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 2Na2O2+2CO2═2Na2CO3+O2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
17.下列关于原电池和电解池的有关说法正确的是( )
| A. | 原电池的负极发生氧化反应,原电池在工作时负极一定溶解 | |
| B. | 以KOH溶液为电解质溶液的甲烷燃料电池工作时,OH-离子从正极移向负极,电解质溶液的PH增大 | |
| C. | 以两个铜棒为电极电解硫酸溶液,在阴极上发生还原反应,且始终是H+在阴极放电生成H2 | |
| D. | 反应2Ag+2HCl═2AgCl+H2↑在电解的条件下可以发生 |
4.下列有关比较中正确的是( )
| A. | 第一电离能:P>S | B. | 气态氢化物的稳定性:CH4>NH3 | ||
| C. | 电负性:CI>F | D. | 最高正化合价:F>S |
1.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 医学上,血液透析是利用了胶体的渗析原理 | |
| B. | 碳酸氢钠可用于制备纯碱,作治疗胃酸过多的药物及食品发酵剂 | |
| C. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 | |
| D. | 二氧化硅是人类将太阳能转换为电能的常用材料 |
2.下列说法正确的是(NA表示阿伏加德罗常数)( )
| A. | 在常温常压下,11.2 升氯气含有的分子数为0.5NA | |
| B. | 1 molFe与足量的Cl2反应转移的电子数为2NA | |
| C. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA | |
| D. | 标准状况下,22.4 LSO3含有的原子数为4NA |