题目内容
11.胶体的性质有:丁达尔现象、布朗运动、电泳现象、聚沉.其中可以用来区分溶液与胶体的是:丁达尔效应.分析 胶体为分散质介于1-100nm的分散系,具有丁达尔现象、布朗运动、电泳现象、聚沉的性质,丁达尔现象是胶体特有性质,据此解答.
解答 解:胶体为分散质介于1-100nm的分散系,具有丁达尔现象、布朗运动、电泳现象、聚沉的性质,丁达尔现象是胶体特有性质,当一束平行光线通过胶体时,从侧面看到一束光亮的“通路”,溶液不具有该性质,可以用来区分溶液与胶体,
故答案为:丁达尔现象、布朗运动、电泳现象、聚沉;丁达尔效应.
点评 本题考查了胶体的性质,侧重考查学生对基础知识掌握的熟练程度,明确胶体的性质是解题关键,注意丁达尔现象是胶体特有性质,题目难度不大.

练习册系列答案
相关题目
16.下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④19.6g H3PO4.
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④19.6g H3PO4.
| A. | ①④③② | B. | ④③②① | C. | ②③④① | D. | ①④②③ |
20.如表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)第3周期中金属性最强的元素是钠(填“钠”或“镁”);
(2)S原子结构示意图为 ;钙离子的电子式为:Ca2+.
;钙离子的电子式为:Ca2+.
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填“H2SO4”或“HClO4”);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;(填“H2S”或“HCl”)
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)N元素形成的一种氢化物其水溶液呈碱性,请写出氢化物的化学式是NH3.
(8)铝是大自然赐予人类的宝物.它其中的一个用途是作为铝热剂,请写出铝和三氧化二铁发生反应的方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)S原子结构示意图为
 ;钙离子的电子式为:Ca2+.
;钙离子的电子式为:Ca2+.(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填“H2SO4”或“HClO4”);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;(填“H2S”或“HCl”)
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)N元素形成的一种氢化物其水溶液呈碱性,请写出氢化物的化学式是NH3.
(8)铝是大自然赐予人类的宝物.它其中的一个用途是作为铝热剂,请写出铝和三氧化二铁发生反应的方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
19.丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图1所示:
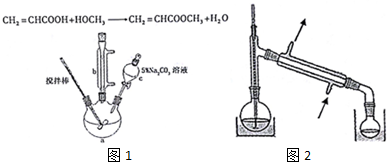
①10.0g丙烯酸和6.0g甲醇放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70-90℃馏分.
可能用到的信息:
回答下列问题:
(1)仪器c的名称是分液漏斗.
(2)混合液用5%0Na2CO3溶液洗涤的目的是除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度).
(3)请写出配制100g 5% Na2CO3溶液所使用的玻璃仪器烧杯、玻璃棒、量筒.
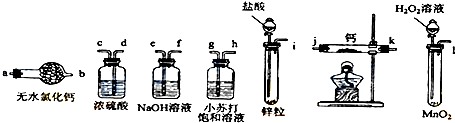
(4)关于产品的蒸馏操作(夹持装置未画出),下图中有2处错误,请分别写出温度计水银球位置、尾接管与锥形瓶接口密封.
为检验产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10-00mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCI溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL.
(5)计算本次酯化反应丙烯酸的转化率54.0%.
(6)请列举2条本实验中需要采取的安全防护措施通风橱中实验、防止明火.

①10.0g丙烯酸和6.0g甲醇放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热.
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性.
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70-90℃馏分.
可能用到的信息:
| 沸点 | 溶解性 | ||
| 丙烯酸 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸丙烯酸甲酯 | 80.5℃ | 难溶于水易溶于有机溶剂 | 易挥发 |
(1)仪器c的名称是分液漏斗.
(2)混合液用5%0Na2CO3溶液洗涤的目的是除去混合液中的丙烯酸和甲醇(降低丙烯酸甲酯的溶解度).
(3)请写出配制100g 5% Na2CO3溶液所使用的玻璃仪器烧杯、玻璃棒、量筒.
(4)关于产品的蒸馏操作(夹持装置未画出),下图中有2处错误,请分别写出温度计水银球位置、尾接管与锥形瓶接口密封.
为检验产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol/L的KOH溶液10-00mL,加热使之完全水解.
②用酚酞做指示剂,向冷却后的溶液中滴加0.5mol/L的HCI溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00mL.
(5)计算本次酯化反应丙烯酸的转化率54.0%.
(6)请列举2条本实验中需要采取的安全防护措施通风橱中实验、防止明火.
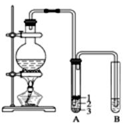 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: