题目内容
17.下列实验过程中,溶液的pH大于7的是( )| A. | 向KNO3溶液中滴加醋酸 | B. | 向KNO3溶液中滴加稀H2SO4 | ||
| C. | 向稀NaCl溶液中滴加稀HNO3 | D. | 向NaCl溶液中滴加Na2CO3溶液 |
分析 溶液的pH大于,说明溶液呈碱性,而KNO3溶液中滴加醋酸、向KNO3溶液中滴加稀H2SO4、向稀NaCl溶液中滴加稀HNO3的混合液都显示酸性只有NaCl溶液中滴加Na2CO3溶液的混合液呈碱性.
解答 解:A.KNO3溶液中滴加醋酸,混合液一定呈酸性,溶液中pH小于7,故A错误;
B.向KNO3溶液中滴加稀H2SO4,混合液一定为酸性,溶液的pH小于7,故B错误;
C.向稀NaCl溶液中滴加稀HNO3,该混合液为酸性,溶液的pH小于7,故C错误;
D.NaCl溶液中滴加Na2CO3溶液,碳酸根离子水解溶液一定呈碱性,溶液的pH大于7,故D正确;
故选D.
点评 本题考查了溶液酸碱性与溶液pH的关系,题目难度不大,明确溶液酸碱性与溶液pH之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
7.500mL NaNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体22.4L(标准状况下),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A. | 原混合溶液中c(Na+)=6 mol | |
| B. | 电解后得到的Cu的物质的量为2 mol | |
| C. | 上述电解过程中共转移8 mol电子 | |
| D. | 电解后溶液中c(H+)=4 mol/L |
8.如图甲、乙是两种重要的有机合成原料.下列有关说法中,不正确的是( )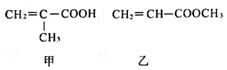
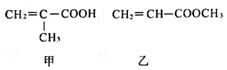
| A. | 甲与乙互为同分异构体 | |
| B. | 甲与乙都能与溴的四氯化碳溶液发生加成反应 | |
| C. | 甲与乙都能与金属钠反应产生氢气 | |
| D. | 在一定条件下,甲与乙均能发生取代反应 |
5.下列关于氢化物的叙述正确的是( )
| A. | 沸点:H2S>HF | B. | 稳定性:H2S<HF | ||
| C. | 一个D2O分子中所含的中子数为8 | D. | HCl的电子式为H+[:Cl:]- |
12.分类是学习和研究化学的一种重要方法.下列分类不合理的是( )
| A. | Na2SiO3和KHCO3都属于盐 | B. | KOH和NH3都属于碱 | ||
| C. | H2SO4和H2S都属于酸 | D. | CaO和NO都属于氧化物 |
2.下列有关17O的说法正确的是??( )
| A. | 质子数为8 | B. | 中子数为8 | C. | 核外电子数为17 | D. | 原子序数为17 |
9.检验SO2中是否含有CO2应采用的方法有( )
| A. | 通过石灰水 | |
| B. | 通过品红溶液 | |
| C. | 先通过小苏打溶液,再通过石灰水 | |
| D. | 先通过足量溴水溶液,再通过石灰水 |
6. 将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
①一定有C2H4
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H2
⑥可能有C3H4
则上述对该混合烃的判断正确的是( )
 将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.
将两种两种气态烃组成的混合气体完全燃烧,得到CO2和H2O的物质量与混合烃的物质的置的关系如图所示.①一定有C2H4
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H2
⑥可能有C3H4
则上述对该混合烃的判断正确的是( )
| A. | ②③⑤ | B. | ⑤⑥ | C. | ②④⑥ | D. | ①④ |
7.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 11.2 LNH3所含分子数为0.5NA | |
| B. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| C. | 23g金属钠与氧气加热生成Na2O2的反应,转移的电子数为2NA | |
| D. | 5.6g铁与足量的盐酸反应,失去的电子数为0.2NA |