题目内容
2.实验室有一包由两种盐(不含氢元素)组成的白色粉末和一瓶标签破损的未知酸溶液.为了确定各自成分,某同学设计了如图实验: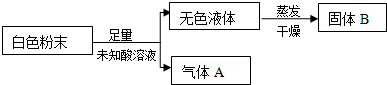
已知,气体A是绿色植物光合作用的原料,固体B是农业上常用的由两种元素组成的钾肥.则:气体A是CO2;未知酸溶液是HCl;组成白色粉末的两种盐是K2CO3和KCl.
分析 由已知条件“气体A是绿色植物光合作用的原料”可知,气体A为二氧化碳;由“固体B是农业上常用的由两种元素组成的钾肥”可知,固体B是氯化钾;然后根据图示逐一推断,即可正确解答.
解答 解:①由“固体B是农业上常用的由两种元素组成的钾肥”可知,固体B是氯化钾;
②因为B是氯化钾,所以无色液体是氯化钾溶液;故未知酸溶液中含有氯离子,故可判断未知酸溶液为盐酸溶液;
③由已知条件“气体A是绿色植物光合作用的原料”可知,气体A为二氧化碳;由此推断白色粉末中含有碳酸跟离子;
④综上所述,白色粉末由氯化钾和碳酸钾这两种盐组成;
⑤氯化钾不能与盐酸发生复分解反应,碳酸钾与盐酸反应的化学方程式为:K2CO3+2HCl=2KCl+H2O+CO2↑.
故答案为:CO2;HCl;K2CO3;KCl.
点评 推断题是中考化学题中的一种常见题型,它涉及的知识面广,题型多样,变化复杂,条件隐蔽,容易出错,是一种既考查知识,又考查能力的题型.
要解答好推断题,应熟练掌握以下几方面:
1.常见物质的性质
2.常见物质的反应规律
3.某些化学反应的特殊现象
解题的关键:是在审题的基础上找准解题的突破口.经过分析,归纳,推理,得出正确的答案.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
17.下列有关金属单质的叙述中,正确的是( )
| A. | 活泼金属在空气中易与氧气反应,都能在其表面形成一层致密的氧化膜 | |
| B. | 钠比铜的活泼性强,所以钠投入到CuSO4溶液中可置换出单质铜 | |
| C. | 等质量的铝粉分别与足量的盐酸或NaOH溶液完全反应时,产生的气体质量相等 | |
| D. | 用铁制或铝制容器来盛装浓硝酸,是因为Fe或Al不能与冷的浓硝酸发生反应 |
10.固体X中可能含有MgCl2、Na2CO3、K2SO3、KAlO2中的一种或几种.为确定该固体粉末的成分,现取X进行下列实验,实验过程及现象如下

根据上述实验,下列说法正确的是( )

根据上述实验,下列说法正确的是( )
| A. | 气体1可能为NO和CO2的混合物 | |
| B. | 沉淀3可能为Mg(OH)2和Al(OH)3的混合物 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
17.现有A、B、C、D、E、F、G七瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Cu(NO3)2和Ba(OH)2溶液中一种.为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示.表中“↓”表示生成沉淀或微溶物,“-”表示观察不到明显变化.
试写出有关物质的化学式:A:KCl,C:MgCl2,E:Cu(NO3)2,G:AgNO3.
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | - | ↓ | ↓ |
| C | - | - | - | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | - | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
7.已知A、B、C、D四种盐,它们分别是CH3COONa、NH4Cl、NaHSO4和BaCl2中的一种,已知A、B溶液的pH相同,A、C混合溶液变浑浊.下列说法正确的是( )
| A. | 熔融态的A中阴离子有2种 | |
| B. | C溶于水会促进水的电离 | |
| C. | 将A溶液滴入B溶液中,能使B溶液中阳离子浓度增大 | |
| D. | B溶液的焰色反应呈黄色 |
14.一包混有杂质的碳酸钠固体,其杂质可能是、Ba(NO3)2、KCl及NaHCO3中的一种或两种,今取样品溶于适量水得到澄清溶液.另取5.3g样品,加入足量的盐酸,收集到2.2gCO2,则下列判断正确的是( )
| A. | 样品中只含有一种杂质NaHCO3 | B. | 样品中含有KCl,不含有NaHCO3 | ||
| C. | 样品中含有Ba(NO3)2和NaHCO3 | D. | 样品中含有KCl和NaHCO3 |
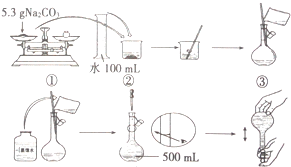 某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol•L-1的Na2CO3溶液.溶液的配制过程如图所示:
某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol•L-1的Na2CO3溶液.溶液的配制过程如图所示: