题目内容
7.已知A、B、C、D四种盐,它们分别是CH3COONa、NH4Cl、NaHSO4和BaCl2中的一种,已知A、B溶液的pH相同,A、C混合溶液变浑浊.下列说法正确的是( )| A. | 熔融态的A中阴离子有2种 | |
| B. | C溶于水会促进水的电离 | |
| C. | 将A溶液滴入B溶液中,能使B溶液中阳离子浓度增大 | |
| D. | B溶液的焰色反应呈黄色 |
分析 根据CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液的酸碱性及A、B溶液的pH相同可以判断出A、B;再根据A、C混合溶液变浑浊可知A、C为硫酸氢钠和氯化钡,二者结合可以推断出A、B、C,据此进行解答本题.
解答 解:有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液的一种:醋酸钠溶液显示碱性、氯化铵显示酸性、硫酸氢钠显示酸性、氯化钡显示中性,由A、B溶液的pH相同,可知A、B为NH4Cl溶液、NaHSO4溶液;A、C混合溶液变浑浊,四种物质中能够生成沉淀的是NaHSO4溶液和BaCl2溶液,根据以上分析可知A为NaHSO4溶液,B为NH4Cl溶液,C为BaCl2溶液,剩下的D为CH3COONa溶液,
A、A为NaHSO4溶液,熔融态的A中阴离子有硫酸氢根离子1种,故A错误;
B、C为氯化钡溶液,氯化钡电离的氯离子和钡离子都不水解,所以氯化钡不影响水的电离,故B错误;
C、A为NaHSO4溶液,B为氯化铵,A加入B中,A电离出的氢离子对B中铵根离子的水解起到抑制作用,所以A能使B溶液中阳离子浓度增大,故C正确;
D、B为NH4Cl溶液,不含钠离子,所以焰色反应不会呈现黄色,故D错误.
故选C.
点评 本题考查了未知物的检验,题目难度不大,涉及了离子反应、弱电解质的电离平衡、盐类水解等知识,试题有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率,该类试题需要注意的是进行物质的检验时,要依据物质的特殊性质和特征反应,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可.

练习册系列答案
相关题目
1.在密闭容器中A和B反应生成C,其反应速率分别用ν(A)、ν(B)、ν(C)表示.已知ν(A)、ν(B)、ν(C)之间有以下关系2ν(B)═3ν(A),2ν(B)═3ν(C),则此反应可表示为( )
| A. | 2A+3B═2C | B. | A+3B═2C | C. | 3A+B═2C | D. | 3A+2B═3C |
2.下列关于燃料电池的说法正确的是( )
| A. | 燃料电池只能在燃烧的情况下才能发生 | |
| B. | 燃料电池是将化学能转化为电能的装置 | |
| C. | 燃料电池属于二次电池的一种 | |
| D. | 燃料电池与燃料燃烧时对能量的转化率完全相同 |
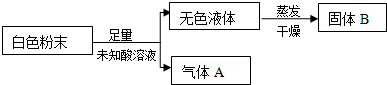
15.有难溶于水的粉末状固体样品,可能含Al、Fe2O3、Cu2O、SiO2、Fe3O4中的一种或几种.研究小组通过实验确定样品的成分.查阅资料知:①Cu2O+2H+═Cu+Cu2++H2O;②部分氢氧化物在溶液中沉淀的pH见表:
注:金属离子的起始浓度为0.1mol•L-1
实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀. 请回答下列问题.
(1)Ⅰ中产生气体的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是SiO2.
(3)溶液C中除H+、Cu2+外一定还含有的阳离子是Fe2+;为验证溶液C中存在该阳离子,可选用的试剂及对应的现象是向酸性KMnO4溶液中滴加待测液,褪色.
(4)Ⅳ中加NaClO的目的是将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀.
(5)由上述实验可以获得结论:原样品所有可能的成分组合为组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4(Al、Fe2O3、Cu2O、Fe3O4); …(用化学式表示,空不够可以补充.)
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀. 请回答下列问题.
(1)Ⅰ中产生气体的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是SiO2.
(3)溶液C中除H+、Cu2+外一定还含有的阳离子是Fe2+;为验证溶液C中存在该阳离子,可选用的试剂及对应的现象是向酸性KMnO4溶液中滴加待测液,褪色.
(4)Ⅳ中加NaClO的目的是将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀.
(5)由上述实验可以获得结论:原样品所有可能的成分组合为组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4(Al、Fe2O3、Cu2O、Fe3O4); …(用化学式表示,空不够可以补充.)
19.下列说法不正确的是( )
| A. | 葡萄糖属于糖类,能发生水解 | |
| B. | 甲烷是最简单的有机化合物 | |
| C. | 油脂有油和脂肪之分,但都属于脂 | |
| D. | 蛋白质、油脂、糖类是三大基本营养物质 |
17.下列说法正确的是( )
| A. | 按系统命名法,有机物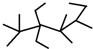 的命名为2,2,4,4,5-五甲基-3,3-二乙基庚烷 的命名为2,2,4,4,5-五甲基-3,3-二乙基庚烷 | |
| B. | 乙醇发生消去反应、乙醇氧化为乙醛、乙酸的酯化反应中均是C-O键发生断裂 | |
| C. | C3H6和C4H8在分子组成上相差CH2,所以二者互为同系物 | |
| D. | 荧光黄结构为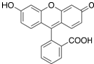 ,其分子式为C20H12O5,其中最多有9个碳原子共平面 ,其分子式为C20H12O5,其中最多有9个碳原子共平面 |
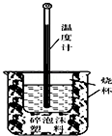 某学习小组的同学在实验室利用如图装置进行中和热的测定.回答下列问题:
某学习小组的同学在实验室利用如图装置进行中和热的测定.回答下列问题: