题目内容
 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )| A、反应开始到第一次平衡时,N2的平均反应速率为 0.005mol/(L?min) |
| B、从曲线变化可以看出,反应进行到10min至20min时可能是使用了催化剂 |
| C、从曲线变化可以看出,反应进行至25min时,分离出0.1mol的氨气 |
| D、在25min时平衡正向移动,但达到新平衡后NH3的体积分数比原平衡小 |
考点:物质的量或浓度随时间的变化曲线,化学平衡的影响因素
专题:化学平衡专题
分析:A.第一次平衡时,时间为20min,氮气的物质的量由0.4mol变为0.25mol,容器容积为2L,根据速率公式可计算出氮气的速率;
B.根据图象知,平衡向正反应方向移动,10min时是连续的,三种气体物质的速率增加倍数相同,说明为使用催化剂;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,压强减小,据此分析.
B.根据图象知,平衡向正反应方向移动,10min时是连续的,三种气体物质的速率增加倍数相同,说明为使用催化剂;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,压强减小,据此分析.
解答:
解:A.第一次平衡时,时间为20min,氮气的物质的量由0.4mol变为0.25mol,容器容积为2L,v(N2)=
=0.00625mol/(L?min),故A错误;
B.由图象可知各组分物质的量变化增加,且10min时变化是连续的,20min达平衡时,△n(N2)=0.4-0.25=0.15mol,△n(H2)=0.6mol-0.15mol=0.45mol,△n(NH3)=0.3mol,物质的量变化之比等于化学计量数之比,三种气体物质的速率增加倍数相同,说明10min可能改变的条件是使用催化剂,故B正确;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,故C正确;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,由于反应条件为恒容,与原平衡相比,容器内压强减小,则反应进行的程度减小,但达到新平衡后NH3的体积分数比原平衡大,故D错误;
故选BC.
| 0.25mol |
| 2L×20min |
B.由图象可知各组分物质的量变化增加,且10min时变化是连续的,20min达平衡时,△n(N2)=0.4-0.25=0.15mol,△n(H2)=0.6mol-0.15mol=0.45mol,△n(NH3)=0.3mol,物质的量变化之比等于化学计量数之比,三种气体物质的速率增加倍数相同,说明10min可能改变的条件是使用催化剂,故B正确;
C.25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,故C正确;
D.第25分钟,NH3的物质的量突然减少,而H2、N2的物质的量不变,说明应是分离出NH3,由于反应条件为恒容,与原平衡相比,容器内压强减小,则反应进行的程度减小,但达到新平衡后NH3的体积分数比原平衡大,故D错误;
故选BC.
点评:本题考查化学平衡的计算、平衡移动以及平衡状态的判断,题目难度中等,注意对图象的分析.

练习册系列答案
相关题目
下列有关氧化还原反应的叙述不正确的是( )
| A、元素化合价发生变化(升高和降低)的反应一定是氧化还原反应 |
| B、在氧化还原反应中一定发生电子转移(电子得失或电子对偏移) |
| C、氧化还原反应一定有氧参加 |
| D、氧化反应和还原反应是同时发生的 |
下列食品添加剂与类别对应正确的一组是( )
| A、着色剂_______苯甲酸钠 |
| B、调味剂_______食盐 |
| C、营养强化剂_______亚硝酸钠 |
| D、防腐剂_______苋菜红 |
下列关于有机物的正确说法是( )
| A、聚乙烯可发生加成反应 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| C、蔗糖及其水解产物均能发生银镜反应 |
| D、C3H8O和C2H6O总质量一定,以任何比例混合,完全燃烧生成CO2与H2O的量为定值 |
下列有关实验的描述中错误的是( )
| A、用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中溶液全部加热蒸干 |
| B、蒸馏操作时,应将温度计水银球置于蒸馏烧瓶的支管口附近 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、使用容量瓶和分液漏斗前,要先检查是否漏水后使用 |
如图所示是配制250mL 1mol/L NaCl溶液时操作.对应操作规范的是( )
A、 称量 称量 |
B、 溶解 |
C、 转移 |
D、 定容 |
下列离子方程式书写不正确的是( )
| A、向氯化铝溶液中加入过量的氨水Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| B、向澄清石灰水中滴加过量碳酸氢钙溶液Ca2++HCO32-+OH-=CaCO3↓+H2O |
| C、向硝酸亚铁溶液中加入稀盐酸3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| D、向硫酸氢钠溶液中加入过量氢氧化钡Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
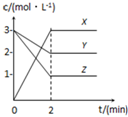 如图表示800℃时,X、Y、Z三种气体物质的浓度随时间变化的情况.试回答:
如图表示800℃时,X、Y、Z三种气体物质的浓度随时间变化的情况.试回答: