题目内容
15.下列有关第ⅦA族元素说法中不正确的是( )| A. | 原子最外层电子数都是7 | B. | 熔、沸点:F2<Cl2<Br2<I2 | ||
| C. | 从F2到I2,颜色逐渐加深 | D. | 从F2到I2,氧化性逐渐增强 |
分析 第ⅦA族元素为卤素,最外层电子数均为7,从上到下非金属性减弱、氧化性减弱,对应单质的颜色加深、熔沸点升高,以此来解答.
解答 解:A.位于第ⅦA族,原子最外层电子数都是7,故A正确;
B.卤素单质均为分子晶体,相对分子质量越大熔沸点越大,则熔、沸点:F2<Cl2<Br2<I2,故B正确;
C.从上到下对应单质的颜色加深,则从F2到I2,颜色逐渐加深,故C正确;
D.从F2到I2,得到电子的能力减小,氧化性逐渐减弱,故D错误;
故选D.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
5.下列说法正确的是( )
| A. | 甲烷的燃烧热为△H=-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 已知H2O(l)═H2O(g)△H=+44 kJ/mol,则2 g H2(g)完全燃烧生成液态水比生成气态水多释放22 kJ的能量 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H<0 | |
| D. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 |
6.用下列实验装置或操作进行的实验能达到实验目的是( )
| A. | 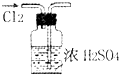 干燥Cl2 | B. | 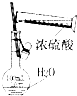 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 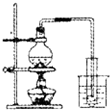 制取少量蒸馏水 | D. | 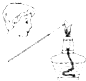 检验钾元素的存在 |
3.常温下,0.2mol•L-1的盐酸30mL分别加适量水与下列Na2CO3溶液混合后,总体积均为100mL,其中最初产生CO2的速率最快的是( )
| A. | 20mL0.3 mol•L-1Na2CO3 | B. | 10mL0.4 mol•L-1Na2CO3 | ||
| C. | 25mL0.4 mol•L-1Na2CO3 | D. | 15mL0.5 mol•L-1Na2CO3 |
10.下列电离方程式错误的是( )
| A. | (NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- | |
| B. | H3PO4溶于水:H3PO4?3H++PO43- | |
| C. | HF溶于水:HF?H++F- | |
| D. | NaHS溶于水:NaHS═Na++HS- |
20.下列说法正确的是( )
| A. | 乙烯的结构简式为CH2CH2,乙烷的结构简式为CH3CH3 | |
| B. | 互为同系物的两种化合物具有相同的最简式,且化学性质相似 | |
| C. | 苯和乙烯都可以与溴水、高锰酸钾溶液反应而使它们褪色 | |
| D. | 乙烯分子中所有原子处于同一平面上,乙烷分子为立体结构,原子不都在同一平面上 |
7.甲醇燃料电池(DMFC)可用于笔记本电脑、汽车等,它一极通入甲醇;电解质是质子交换膜,它能传导氢离子.电池工作时,甲醇被氧化为二氧化碳和水.下列叙述中,不正确的是( )
| A. | 负极的反应式为:CH3OH+H2O-6e-═CO2↑+6H+ | |
| B. | 氧气在电极上的反应是O2+4H++4e-═2H2O | |
| C. | 通入甲醇的一极为负极,通入氧气的一极为正极 | |
| D. | 燃料电池的能量转化率能达到100% |