题目内容
19.NA表示阿伏伽德罗常数,1molNaOH固体含有( )| A. | NA个OH- | B. | 3NA个离子 | C. | 2NA原子 | D. | 10NA个电子 |
分析 NaOH固体是离子晶体,构成微粒为钠离子和氢氧根离子.
解答 解:A、1mol中NaOH含有1mol的钠离子和1mol的氢氧根离子,所以含NA个氢氧根离子,故A正确;
B、1mol中NaOH含有1mol的钠离子和1mol的氢氧根离子,故含2mol离子即2NA个,故B错误;
C、1mol氢氧化钠中含3mol原子即3NA个,故C错误;
D、1mol的钠离子含有10NA个电子和1mol的氢氧根离子含有10NA个电子,所以共有20NA个电子,故D错误;
故选A.
点评 本题考查学生物质的组成知识,可以根据所学知识进行回答,难度不.

练习册系列答案
相关题目
7.纯过氧化氢是淡蓝色的粘稠液体,可与水以任意比混合,水溶液俗称双氧水,为无色透明液体.实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等.某化学兴趣小组的同学绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学校认为:
(1)写出过氧化氢的电子式 ;
;
(2)实验室中用过氧化氢制取氧气的化学方程式为2H2O2$\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,当生成标准状况下2.24LO2时,转移电子为0.2mol;
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱.请写出H2O2在其水溶液中的电离方程式H2O2?HO2-+H+,HO2-?H++O22-;
(4)同学们用0.1000mol•L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,其反应原理为2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2.
①在该反应中,H2O2被氧化(填“氧化”或“还原”)
②滴定到达终点的现象是锥形瓶内溶液颜色恰好由无色变为浅紫色,且30秒内溶液不褪色;
③用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的KMnO4标准溶液体积如下表所示:
则试样中过氧化氢的浓度为0.1800mol•L-1;
④若滴定前尖嘴中有气泡,滴定后消失,则滴定结果偏高(填“偏低”、“偏高”或“不变”);
(5)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失.关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色.请设计一个简单的实验方案来判断甲乙两位同学的说法是否正确:在褪色后的溶液中,加入适量的NaOH溶液,若又出现红色,则甲同学的观点正确;若未出现红色,则乙同学的观点正确.
(1)写出过氧化氢的电子式
 ;
;(2)实验室中用过氧化氢制取氧气的化学方程式为2H2O2$\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,当生成标准状况下2.24LO2时,转移电子为0.2mol;
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱.请写出H2O2在其水溶液中的电离方程式H2O2?HO2-+H+,HO2-?H++O22-;
(4)同学们用0.1000mol•L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,其反应原理为2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2.
①在该反应中,H2O2被氧化(填“氧化”或“还原”)
②滴定到达终点的现象是锥形瓶内溶液颜色恰好由无色变为浅紫色,且30秒内溶液不褪色;
③用移液管吸取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗的KMnO4标准溶液体积如下表所示:
 | 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
④若滴定前尖嘴中有气泡,滴定后消失,则滴定结果偏高(填“偏低”、“偏高”或“不变”);
(5)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失.关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色.请设计一个简单的实验方案来判断甲乙两位同学的说法是否正确:在褪色后的溶液中,加入适量的NaOH溶液,若又出现红色,则甲同学的观点正确;若未出现红色,则乙同学的观点正确.
14.下列微粒中,最重的是( )
| A. | α粒子 | B. | 质子 | C. | 中子 | D. | ${\;}_{1}^{1}$ H |
4. 为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去).请回答下列问题:
为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去).请回答下列问题:
(1)仪器A的名称球形冷凝管,其作用是冷凝回流溴,以免溴挥发.
(2)用仪器B滴加液体并不需要打开玻璃塞c,原因是滴液漏斗和三颈瓶相通,气压相等.
(3)实验记录如下(请补全空白):
(4)步骤Ⅱ中,开始时颜色无明显变化的原因是(写出一条)步骤1的H2SO3有过量,H2O2先和H2SO3反应,
步骤Ⅰ中反应的离子方程式H2SO3+Br2+H2O=4H++SO42-+2Br-,
步骤Ⅱ中主要反应的离子方程式H2O2+2Br-+2H+=Br2+2H2O.
 为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去).请回答下列问题:
为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去).请回答下列问题:(1)仪器A的名称球形冷凝管,其作用是冷凝回流溴,以免溴挥发.
(2)用仪器B滴加液体并不需要打开玻璃塞c,原因是滴液漏斗和三颈瓶相通,气压相等.
(3)实验记录如下(请补全空白):
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 打开活塞a,逐滴加入H2SO3溶液至过量 | 橙黄色褪去 | Br2的氧化性大于H2SO3 |
| Ⅱ | 向步骤Ⅰ所得溶液中逐滴加入H2O2溶液 | 刚开始溶液颜色无明显变化,继续滴加,溶液变为橙黄色 | H2O2的氧化性大于Br2 |
步骤Ⅰ中反应的离子方程式H2SO3+Br2+H2O=4H++SO42-+2Br-,
步骤Ⅱ中主要反应的离子方程式H2O2+2Br-+2H+=Br2+2H2O.
11.下列属于氧化还原反应的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | 2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | ||
| C. | SO3+H2O═H2SO4 | D. | NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ |
9.碳酸镁晶须是一种新型吸波隐形材料中的增强剂.某工厂以MgCl2(含少量杂质FeCl2、FeCl3)为原料制备碳酸镁晶须(MgCO3•H2O)的工艺流程如下:
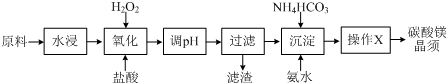
已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
注:Fe(OH)2沉淀呈絮状,不易从溶液中除去.
(1)写出“氧化”过程中发生的离子反应方程式并用单线桥标出电子转移的方向和数目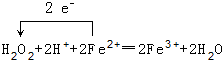 .
.
(2)pH调节的范围3.7~9.9之间,滤渣的主要成分Fe(OH)3(填化学式).
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法取最后一次洗涤液,加入硝酸酸化,再加入硝酸银溶液,没有白色沉淀生成,说明洗涤干净.
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00mL,测得Cl-的浓度为0.455mol•L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460mol•L-1(溶液体积变化忽略不计).
②另取水浸后溶液100.00mL,向其中加入过量的1mol•L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96g.
试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程).

已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mg(OH)2 | 9.9 | 11.1 |
(1)写出“氧化”过程中发生的离子反应方程式并用单线桥标出电子转移的方向和数目
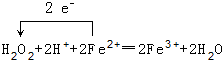 .
.(2)pH调节的范围3.7~9.9之间,滤渣的主要成分Fe(OH)3(填化学式).
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法取最后一次洗涤液,加入硝酸酸化,再加入硝酸银溶液,没有白色沉淀生成,说明洗涤干净.
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00mL,测得Cl-的浓度为0.455mol•L-1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl-的浓度为0.460mol•L-1(溶液体积变化忽略不计).
②另取水浸后溶液100.00mL,向其中加入过量的1mol•L-1NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96g.
试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度(写出计算过程).