题目内容
下列描述正确的是( )
| A、在pH=1溶液中,NH+4、K+、ClO-、Cl-可以大量共存 |
| B、MgO可以除去MgCl2溶液中的FeCl3 |
| C、足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、向某溶液滴加盐酸酸化的氯化钡溶液,出现白色沉淀,则证明该溶液中含有SO42- |
考点:离子共存问题,离子方程式的书写,硫酸根离子的检验
专题:离子反应专题
分析:A.pH=1溶液,显酸性,离子之间发生氧化还原反应;
B.MgO可促进氯化铁的水解;
C.反应生成硝酸亚铁;
D.白色沉淀可能为AgCl.
B.MgO可促进氯化铁的水解;
C.反应生成硝酸亚铁;
D.白色沉淀可能为AgCl.
解答:
解:A.pH=1溶液,显酸性,H+、ClO-、Cl-离子之间发生氧化还原反应,不能大量共存,故A错误;
B.MgO可促进氯化铁的水解生成氢氧化铁沉淀,则MgO可以除去MgCl2溶液中的FeCl3,故B正确;
C.反应生成硝酸亚铁,则离子反应为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C错误;
D.白色沉淀可能为AgCl,也可能为硫酸钡,则不能证明该溶液中含有SO42-,还可能为银离子,但二者不能同时存在,故D错误;
故选B.
B.MgO可促进氯化铁的水解生成氢氧化铁沉淀,则MgO可以除去MgCl2溶液中的FeCl3,故B正确;
C.反应生成硝酸亚铁,则离子反应为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故C错误;
D.白色沉淀可能为AgCl,也可能为硫酸钡,则不能证明该溶液中含有SO42-,还可能为银离子,但二者不能同时存在,故D错误;
故选B.
点评:本题考查较综合,涉及离子共存、离子反应及离子检验等,注重高频考点的考查,把握离子之间的反应为解答的关键,题目难度不大.

练习册系列答案
相关题目
下列仪器:①烧杯;②蒸发皿;③表面皿;④烧瓶;⑤坩埚;⑥容量瓶;⑦量筒.能用酒精灯加热的是( )
| A、①②④⑤ | B、①③④⑤ |
| C、②③⑤⑥ | D、②③⑥⑦ |
两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是( )
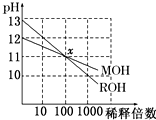

| A、ROH是一种强碱 |
| B、在x点,c(M+)=c(R+) |
| C、在x点,ROH完全电离 |
| D、稀释前,c(ROH)=10 c(MOH) |
下列与有机物结构、性质相关的叙述正确的是( )
| A、乙醇分子和水分子中都含有羟基,均可与金属钠反应生成氢气 |
| B、苯和乙烯分别与酸性高锰酸钾溶液混合,现象相同 |
| C、淀粉和纤维素均为多糖,属于同分异构体 |
| D、石油的分馏、煤的干馏、煤的气化和液化均为物理变化 |
铝、铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低.已知反应:BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是( )
| A、Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO |
| B、BeCl2溶液的pH>7,将其蒸干并灼烧后得到的残留物可能是BeCl2 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、BeCl2水溶液的导电性强,故BeCl2是离子化合物 |
一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A、2 mol SO2+1 mol O2 |
| B、4 mol SO2+1 mol O2 |
| C、2 mol SO2+1 mol O2+2 SO3 |
| D、3 mol SO2+1 mol O2+1 SO3 |
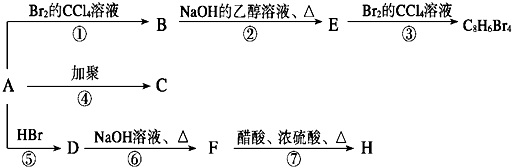
 (主要产物),1mol某芳香烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下面所示的一系列变化.
(主要产物),1mol某芳香烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下面所示的一系列变化.