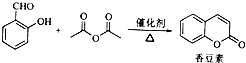
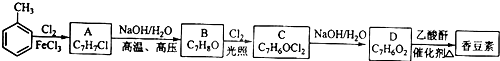
题目内容
将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:2CH3COOK+2H2O
CH3CH3↑+2CO2↑+H2↑+2KOH
现有下列衍变关系(A、B、C、D、E、F、G均为有机物):
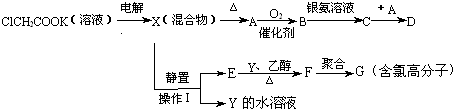
回答下列问题:
(1)写出电解ClCH2COOK溶液时的阳极的电极反应式 ;
(2)操作Ⅰ的名称是 ,G的结构简式是 ;
(3)写出B与银氨溶液按物质的量1:4反应生成C的化学方程式: ;
(4)A和C在不同条件下反应,会生成不同的D,若D的相对分子质量是B的2倍,则D的结构简式是 .
| 电解 |
现有下列衍变关系(A、B、C、D、E、F、G均为有机物):

回答下列问题:
(1)写出电解ClCH2COOK溶液时的阳极的电极反应式
(2)操作Ⅰ的名称是
(3)写出B与银氨溶液按物质的量1:4反应生成C的化学方程式:
(4)A和C在不同条件下反应,会生成不同的D,若D的相对分子质量是B的2倍,则D的结构简式是
考点:有机物的推断
专题:有机物的化学性质及推断
分析:由题目信息可知,电解ClCH3COOK溶液得到ClCH2CH2Cl、KOH混合溶液,加热ClCH2CH2Cl发生水解得到A为HOCH2CH2OH,乙二醇发生催化氧化生成B为OHC-CHO,乙二醛与银氨溶液发生氧化反应C为HOOC-COOH,乙二酸与乙二醇发生酯化反应生成D,若D的相对分子质量是B的2倍,则D的结构简式是 ,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为
,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为 ,据此解答.
,据此解答.
 ,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为
,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为 ,据此解答.
,据此解答.解答:
解:由题目信息可知,电解ClCH3COOK溶液得到ClCH2CH2Cl、KOH混合溶液,加热发生水解得到A为HOCH2CH2OH,乙二醇发生催化氧化生成B为OHC-CHO,乙二醛与银氨溶液发生氧化反应C为HOOC-COOH,乙二酸与乙二醇发生酯化反应生成D,若D的相对分子质量是B的2倍,则D的结构简式是 ,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为
,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为 ,
,
(1)电解ClCH2COOK溶液时,阳极发生氧化反应,ClCH2COO-在阳极放电生成ClCH2CH2Cl、CO2,阳极电极反应式为:2ClCH2COO--2e-=ClCH2CH2Cl+2CO2↑,故答案为:2ClCH2COO--2e-=ClCH2CH2Cl+2CO2↑;
(2)操作Ⅰ是分离互不相溶的液体,应采取分液方法分离,G的结构简式是 ,故答案为:分液;
,故答案为:分液; ;
;
(3)B为OHC-CHO,与银氨溶液按物质的量1:4反应生成C的化学方程式: ,
,
故答案为: ;
;
(4)乙二酸与乙二醇发生酯化反应生成D,若D的相对分子质量是OHC-CHO的2倍,则D的结构简式是 ,故答案为:
,故答案为: .
.
 ,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为
,ClCH2CH2Cl不溶于水,静置,分液得到Y为KOH,E为ClCH2CH2Cl,E在KOH、乙醇、加热条件下发生消去反应生成F,F发生加聚反应生成含氯高分子,则F为CH2=CHCl,G为 ,
,(1)电解ClCH2COOK溶液时,阳极发生氧化反应,ClCH2COO-在阳极放电生成ClCH2CH2Cl、CO2,阳极电极反应式为:2ClCH2COO--2e-=ClCH2CH2Cl+2CO2↑,故答案为:2ClCH2COO--2e-=ClCH2CH2Cl+2CO2↑;
(2)操作Ⅰ是分离互不相溶的液体,应采取分液方法分离,G的结构简式是
 ,故答案为:分液;
,故答案为:分液; ;
;(3)B为OHC-CHO,与银氨溶液按物质的量1:4反应生成C的化学方程式:
 ,
,故答案为:
 ;
;(4)乙二酸与乙二醇发生酯化反应生成D,若D的相对分子质量是OHC-CHO的2倍,则D的结构简式是
 ,故答案为:
,故答案为: .
.
点评:本题考查有机物推断,关键是根据反应信息确定电解ClCH3COOK溶液得到ClCH2CH2Cl、KOH混合溶液,再结合反应条件进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
下列描述正确的是( )
| A、在pH=1溶液中,NH+4、K+、ClO-、Cl-可以大量共存 |
| B、MgO可以除去MgCl2溶液中的FeCl3 |
| C、足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D、向某溶液滴加盐酸酸化的氯化钡溶液,出现白色沉淀,则证明该溶液中含有SO42- |
用浓H2SO4跟分子式分别为C2H6O和C3H8O的醇的混合液反应,可得到醚的种类有( )
| A、1种 | B、3种 | C、5种 | D、6种 |