题目内容
用下列实验装置进行相应的实验,能达到实验目的是( )
A、 利用如图装置制取并收集干燥纯净的NH3 |
B、 利用如图所示装置制备可除去NO2中的NO |
C、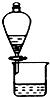 利用如图装置可分离CH3COOC2H5和饱和碳酸钠溶液 |
D、 利用如图装置制备Fe(OH)2并能较长时间观察其颜色 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.氨气密度比空气小,应用向下排空法收集;
B.二氧化氮与水反应生成一氧化氮;
C.CH3COOC2H5不溶于饱和碳酸钠溶液;
D.铁应为阳极,被氧化生成Fe2+.
B.二氧化氮与水反应生成一氧化氮;
C.CH3COOC2H5不溶于饱和碳酸钠溶液;
D.铁应为阳极,被氧化生成Fe2+.
解答:
解:A.气体收集错误,氨气密度比空气小,应用向下排空法收集,故A错误;
B.二氧化氮与水反应生成一氧化氮,应与适量氧气反应,故B错误;
C.CH3COOC2H5不溶于饱和碳酸钠溶液,可用分液的方法分离,故C正确;
D.铁应为阳极,被氧化生成Fe2+,进而生成Fe(OH)2,故D错误.
故选C.
B.二氧化氮与水反应生成一氧化氮,应与适量氧气反应,故B错误;
C.CH3COOC2H5不溶于饱和碳酸钠溶液,可用分液的方法分离,故C正确;
D.铁应为阳极,被氧化生成Fe2+,进而生成Fe(OH)2,故D错误.
故选C.
点评:本题考查较为综合,涉及物质的分离、制备以及气体的收集等知识,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性、可行性的评价,难度中等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列说法正确的是( )
| A、化学反应能够制造新物质,同时也能制造出新的元素 |
| B、煤在空气中强热得到焦炭、煤焦油、焦炉气、粗氨水等产物的过程叫煤的干馏 |
| C、在酿酒的过程中,葡萄糖可通过水解反应生成酒精 |
| D、工业生产玻璃、水泥、冶炼铁均需要用到石灰石为原料 |
初步提纯下列物质(括号内为少量杂质),选用的试剂和分离方法均正确的是( )
| 序号 | 物质 | 试剂 | 分离方法 |
| ① | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ② | 乙烷(乙烯) | 氢气 | 洗气 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(环己烷) | 水 | 分液 |
| A、①② | B、①③ | C、③ | D、④③ |
下列物质中,不能使酸性KMnO4溶液褪色的物质是( )
① ②乙烯 ③CH3COOH
②乙烯 ③CH3COOH
④CH3CH2OH ⑤CH2═CH-COOH ⑥
①
 ②乙烯 ③CH3COOH
②乙烯 ③CH3COOH④CH3CH2OH ⑤CH2═CH-COOH ⑥

| A、①⑤ | B、①②④⑥ |
| C、①④ | D、①③⑥ |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,104 g苯乙烯中含有的碳碳双键数为NA |
| B、5.6克铁与足量盐酸反应,转移0.3NA个电子 |
| C、2mol的甲基(-CH3)所含电子数为14NA |
| D、标准状况下,22.4L辛烷完全燃烧生成二氧化碳分子数为8NA |
常温下,下列溶液中各粒子的物质的量浓度关系正确的是( )
| A、0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
| B、相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ |
| C、0.2 mol/L的NaHCO3溶液与0.3mol/L的Ba(OH)2溶液等体积混合,所得溶液中:c(OH-)>c(Ba2+)>c(Na+)>c(H+) |
| D、等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A、一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA |
| B、256g S8分子中含S-S键为7NA个 |
| C、由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| D、1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 |
