题目内容
某含氧有机化合物A.它的相对原子质量为88.0.含C的质量分数为68.2%,含H的质量分数为13.6%.
(1)通过计算推导出A的分子式;
(2)经红外光谱测定A中含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同的环境的氢原子,写出A的结构简式;
(3)A与乙醇互为 .
(1)通过计算推导出A的分子式;
(2)经红外光谱测定A中含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同的环境的氢原子,写出A的结构简式;
(3)A与乙醇互为
考点:有关有机物分子式确定的计算
专题:
分析:(1)根据有机物各元素的质量分数计算原子个数比值,求出最简式,根据相对分子质量计算出该有机物的化学式;
(2)根据结构特点书写结构简式;
(3)根据乙醇与A的结构简式判断二者关系.
(2)根据结构特点书写结构简式;
(3)根据乙醇与A的结构简式判断二者关系.
解答:
解:(1)N(C):N(H):N(O)=
:
:
=5:12:1,即该有机化合物的最简式为:C5H12O,设其组成为(C5H12O)n,则(5×12+12×1+16)n=88.0,解得n=1,有机物的分子式为:C5H12O,
答:A的分子式为C5H12O;
(2)经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同环境的H原子,则其结构简式为: ,
,
答:A的结构简式为 ;
;
(3)A的结构简式为 ,与乙醇具有相似结构,分子间相差2个CH2原子团,所以二者互为同系物,
,与乙醇具有相似结构,分子间相差2个CH2原子团,所以二者互为同系物,
故答案为:同系物.
| 68.2% |
| 12 |
| 13.6% |
| 1 |
| 1-68.2%-13.6% |
| 16 |
答:A的分子式为C5H12O;
(2)经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同环境的H原子,则其结构简式为:
 ,
,答:A的结构简式为
 ;
;(3)A的结构简式为
 ,与乙醇具有相似结构,分子间相差2个CH2原子团,所以二者互为同系物,
,与乙醇具有相似结构,分子间相差2个CH2原子团,所以二者互为同系物,故答案为:同系物.
点评:本题考查了常见有机物分子式的计算,题目难度中等,注意掌握质量守恒定律在确定有机物分子式中的应用,明确掌握常见有机物结构与性质.

练习册系列答案
相关题目
M、X、Y、Z、W是原子序数依次递增的五种短周期元素,M是所有元素中原子半径最小的,X的一种单质是自然界中硬度最高的物质,Z、W同主族且能形成多种常见化合物.下列叙述正确的是( )
| A、稳定性:W的氢化物>Z的氢化物,沸点:W的氢化物<Z的氢化物 |
| B、元素X、Y、Z的单质晶体可能属于同种类型的晶体 |
| C、XZ2、X2M2、M2Z2均为直线型的共价化合物 |
| D、由Z和W组成的一种化合物能使酸性高锰酸钾溶液褪色,表明其具有漂白性 |
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)( )
A、 实验室用乙醇制取乙烯 |
B、 实验室制取乙酸乙酯 |
C、 石油分馏 |
D、 实验室制取硝基苯 |
用下列实验装置进行相应的实验,能达到实验目的是( )
A、 利用如图装置制取并收集干燥纯净的NH3 |
B、 利用如图所示装置制备可除去NO2中的NO |
C、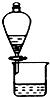 利用如图装置可分离CH3COOC2H5和饱和碳酸钠溶液 |
D、 利用如图装置制备Fe(OH)2并能较长时间观察其颜色 |
下列物质无法从海水中获得的是( )
| A、硫酸 | B、氯化镁 |
| C、溴 | D、氢氧化钠 |
下列有关实验原理或操作方法正确的是( )
| A、在漂白粉中滴入70%的硫酸,立即产生黄绿色气体,说明硫酸具有还原性 |
| B、实验室从海带中提取单质碘的方法:取样→灼烧→溶解→过滤→萃取 |
| C、燃料电池制作实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果更好 |
| D、润洗滴定管时应从滴定管上口加入润洗溶液,倾斜着转动滴定管使液体润湿内壁,再从上口倒出,重复2-3次 |
聚乳酸的结构为 有机物的相关叙述正确的是( )
有机物的相关叙述正确的是( )
 有机物的相关叙述正确的是( )
有机物的相关叙述正确的是( )| A、其单体不能发生消去反应 |
| B、其单体可以通过反应形成六元环状化合物 |
C、其单体含有 |
| D、聚乳酸是由加聚反应获得 |
六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E、B与F同主族;E与F同周期;D的核电荷数是F的最外层电子数的2倍;B的最高正价与最低负价的代数和为0;常温下单质A与E的状态不同.下列推断正确的是( )
| A、A、C两种元素可组成化学式为CA3的化合物 |
| B、F与D形成的化合物性质很不活泼,不与任何酸反应 |
| C、原子半径由大到小的顺序为F>E>A |
| D、元素的非金属由强到弱的顺序为D>C>F>B |
