题目内容
17.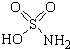 氨基磺酸(结构如图所示)是一种强酸,工业上用于酸性清洗剂、磺化剂等.加热至60℃时与水反应生成一种盐,该盐的溶液呈强酸性.下列有关氨基磺酸说法正确的是( )
氨基磺酸(结构如图所示)是一种强酸,工业上用于酸性清洗剂、磺化剂等.加热至60℃时与水反应生成一种盐,该盐的溶液呈强酸性.下列有关氨基磺酸说法正确的是( )| A. | 不溶于水 | B. | 不能清洗铁锈 | ||
| C. | 水溶液中以分子形式大量存在 | D. | 与水反应生成的盐是NH4HSO4 |
分析 A.氨基和磺酸基易溶于水;
B.氨基磺酸是一种强酸;
C.氨基磺酸是一种强酸,可电离;
D.氨基磺酸水溶液加热至60度以上时,将水解成硫酸盐.
解答 解:A.氨基和磺酸基易溶于水,氨基磺酸易溶于水,故A错误;
B.氨基磺酸是一种强酸可与铁锈反应,故B错误;
C.氨基磺酸是一种强酸,可完全电离,以离子形式存在,故C错误;
D.氨基磺酸水溶液加热至60度以上时,将水解成NH4HSO4,故D正确.
故选D.
点评 本题考查有机物的结构与性质,注意习题中的信息分析物质的性质,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
相关题目
7.科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,有关他们的叙述正确的是( )
①互为同素异形体 ②属于同一种物质 ③富勒烯和足量氧气充分反应,最终产物不同④富勒烯都可以发生加成反应 ⑤富勒烯在苯中溶解度比在乙醇中溶解度大.
①互为同素异形体 ②属于同一种物质 ③富勒烯和足量氧气充分反应,最终产物不同④富勒烯都可以发生加成反应 ⑤富勒烯在苯中溶解度比在乙醇中溶解度大.
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ①④⑤ | D. | ①③④⑤ |
8.下列溶液中相应关系正确的是( )
| A. | 0.2 mol•L-1CH3COONa溶液和0.1 mol•L-1HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | pH=3的盐酸和NaOH的混合溶液中:c(Na+)=c(Cl-) | |
| C. | 0.1 mol•L-1NaHCO3 溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 含SO42-、NH4+、H+、OH-的溶液中可能存在:c(H+)>c(SO42-)>c(NH4+)>c(OH-) |
5.下列实验操作中,正确的是( )
| A. | 配制100mL2mol/LNaCl溶液,将称量的NaCl放入烧杯中加20-30mL的蒸馏水搅拌溶解 | |
| B. | 蒸馏操作时,应将温度计插入烧瓶中的溶液中 | |
| C. | 测溶液的pH时,将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 | |
| D. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
9.常温下加入下列物质,能使溶液中c(CO32-)、c(HCO3-)均降低,而pH增大的是( )
| A. | 氢氧化钠溶液 | B. | 通入二氧化碳 | C. | 氢氧化钙溶液 | D. | 盐酸 |
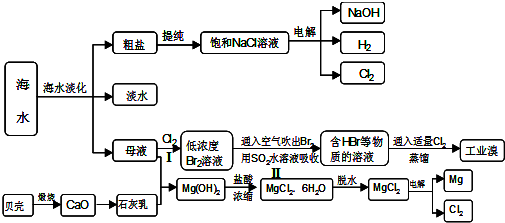
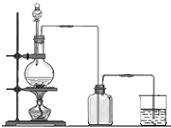 实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答:
实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答:
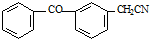 ;由C→D的反应类型是取代反应.
;由C→D的反应类型是取代反应.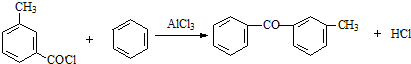 .
. .
. 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$\stackrel{NaOH溶液}{→}$CH3CH2OH
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$\stackrel{NaOH溶液}{→}$CH3CH2OH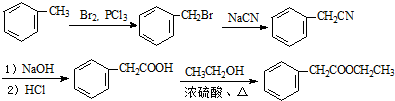 .
.