题目内容
2.胡椒酚是植物挥发油中的一种成分.关于胡椒酚(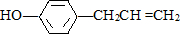 )的下列说法中正确的是( )
)的下列说法中正确的是( )| A. | 该化合物属于芳香烃 | |
| B. | 分子中至少有7个碳原子处于同一个平面 | |
| C. | 它的部分同分异构体能与碳酸氢钠溶液反应产生气体 | |
| D. | 1mol该化合物最多可与2molBr2发生反应 |
分析 该物质中含有苯环、酚羟基和碳碳双键,具有苯、酚和烯烃的性质,能发生加成反应、取代反应、氧化反应、缩聚反应、加聚反应等,据此分析解答.
解答 解:A.该化合物中除了含有C、H元素之外还有O元素,所以属于烃的含氧衍生物而不属于烃,故A错误;
B.根据苯和乙烯结构知,分子中至少有苯环上和连接苯环的碳原子7个碳原子处于同一个平面,故B正确;
C.只有羧基能和碳酸氢钠反应生成二氧化碳气体,该物质中只有一个O原子,所以其同分异构体中没有含有羧基,所以不能和碳酸氢钠反应,故C错误;
D.碳碳双键能和溴发生加成反应,苯环上酚羟基的邻位H原子能和溴发生取代反应,所以1mol该化合物最多可与3molBr2发生反应,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚和烯烃性质,注意酚和溴发生取代反应位置,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.${\;}_{\;}^{16}$O和${\;}_{\;}^{18}$O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | ${\;}_{\;}^{16}$O2与${\;}_{\;}^{18}$O2是氧元素的两种核素 | |
| B. | 标准状况下,1.12L${\;}_{\;}^{16}$O2和1.12L${\;}_{\;}^{18}$O2均含有0.1NA个氧原子 | |
| C. | 通过化学变化可以实现${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O之间的相互转化 | |
| D. | ${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O核外电子排布方式不同 |
13.用惰性电解电解一定体积的CuSO4溶液一段时间后,发现需加入0.15mol Cu(OH)2才能使溶液恢复到原来状态,则整个电解过程中转移的电子的物质的量为( )
| A. | 0.3mol | B. | 0.4mol | C. | 0.5mol | D. | 0.6mol |
7.已知反应:3A+4B?C+2D 其反应速率可以分别用V(A)、V(B)、V(C)、V(D)[mol/(L•min)]表示,则正确的关系是( )
| A. | V(A)=$\frac{1}{3}$V(C) | B. | V(B)=$\frac{4}{3}$V(A) | C. | V(C)=4V(B) | D. | V(D)=2V(C) |
14.为了得到比较纯净的物质,下列使用的方法恰当的是( )
| A. | 向Na2CO3饱和溶液中,通入过量的CO2后,加热蒸干得NaHCO3晶体 | |
| B. | 加热蒸发CuCl2饱和溶液得纯净的CuCl2晶体 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 向FeCl3溶液里加入足量NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3 |
11.下列说法中正确的是( )
| A. | 化学性质相似的有机物一定互为同系物 | |
| B. | 分子组成相差一个或几个CH2原子团的有机物一定互为同系物 | |
| C. | 同系物之间相对分子质量一定相差14的整数倍 | |
| D. | 互为同系物的有机化合物可能互为同分异构体 |
12.NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,请根据题意回答下列问题:
Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ 2CO2(g)+N2(g)△H=-748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
(1)前2s内的平均反应速率υ(N2)=2.08×10-4mol/(L•s)(保留3位有效数字,下同);计算此温度下该反应的K=3.65×106.
(2)达到平衡时,下列措施能提高NO转化率的是BD.(填字母序号)
A.选用更有效的催化剂B.降低反应体系的温度
C.充入氩气使容器内压强增大D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为284kJ/mol或△H=-284kJ/mol.
Ⅱ.臭氧也可用于处理NO.
(4)O3氧化NO结合水洗可产生HNO3和O2,每生成1mol的HNO3转移3mol电子.
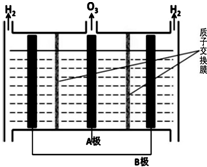
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为B(填“A”或“B”),阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+.
Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ 2CO2(g)+N2(g)△H=-748kJ/mol
为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
(2)达到平衡时,下列措施能提高NO转化率的是BD.(填字母序号)
A.选用更有效的催化剂B.降低反应体系的温度
C.充入氩气使容器内压强增大D.充入CO使容器内压强增大
(3)已知N2(g)+O2(g)=2NO(g)△H=+180kJ/mol;则CO的燃烧热为284kJ/mol或△H=-284kJ/mol.
Ⅱ.臭氧也可用于处理NO.
(4)O3氧化NO结合水洗可产生HNO3和O2,每生成1mol的HNO3转移3mol电子.
(5)O3可由电解稀硫酸制得,原理如图.图中阴极为B(填“A”或“B”),阳极(惰性电极)的电极反应式为3H2O-6e-=O3+6H+.

 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)(需要写出简单的求解步骤)
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)(需要写出简单的求解步骤)
 ,A的电子式为
,A的电子式为 .
. +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.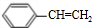 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$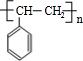 .
.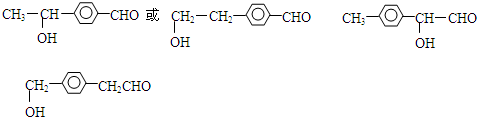 任意一种.(写出一种即可)
任意一种.(写出一种即可)