题目内容
15.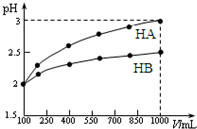 已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示.
已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示.(1)常温下,NaB溶液的pH>7(填“>”、“<”或“=”).
原因用离子方程式表示为B-+H2O?HB+OH-;
(2)某温度下,0.01mol/LHB与0.01mol/L NaOH以体积比2:1 混合后溶液呈酸性,PH=5,则下列关系一定正确的是ABC
A.c(H+)+c(Na+)=c(OH-)+c(B-)
B.c(Na+)=2[c(HB)+c(B-)]
C.c(Na+)>c(HB)
D.c(OH-)=10-9 mol/L
(3)已知常温下HA、HB的难溶的银盐(AgA、AgB)饱和溶液中存在以下平衡:AgA(s)?Ag+(aq)+A-(aq) Ksp(AgA )=2.1×10-10、AgB(s)?Ag+(aq)+B-(aq) Ksp(AgB )=1.0×10-2
AgNO3溶液中加入 NaA、NaB溶液,当两种沉淀共存时,$\frac{c({A}^{-})}{c({B}^{-})}$=2.1×10-8.
分析 (1)加水至1000mL时,A的pH=3,说明A为强酸,而B的pH小于3,应为弱酸,结合盐的水解原理的解答该题;
(2)0.01mol/LHB与0.01mol/LNaOH以体积比2:1混合后溶液是等浓度的NaB和HB的混合物,溶液呈酸性,所以酸的电离程度大于弱离子的水解程度;
(3)向AgNO3溶液中加入 NaA、NaB溶液,当两种沉淀共存时依据AgA和AgB的溶度积可知,AgB溶解度大于AgA,依据氯二者的溶度积计算和沉淀转化关系计算得到.
解答 解:(1)加水至1000mL时,A的pH=3,说明A为强酸,而B的pH小于3,应为弱酸,NaB属于强碱弱酸盐,弱离子水解使得溶液的pH>7,B-+H2O?HB+OH-,故答案为:>;B-+H2O?HB+OH-;
(2)0.01mol/LHB与0.01mol/LNaOH以体积比2:1混合后溶液是等浓度的NaB和HB的混合物,溶液呈酸性,所以酸的电离程度大于弱离子的水解程度.
A.电荷守恒:c(H+)+c(Na+)=c(OH-)+c(B-),故A正确;
B.存在物料守恒:c(Na+)=2[c(HB)+c(B-)],故B正确;
C.酸的电离程度大于弱离子的水解程度,所以:c(Na+)>c(HB),故C正确;
D.混合后溶液呈酸性PH=5,但是温度不定,所以无法确定c(OH-),故D错误.
故选ABC.
(3)向AgNO3溶液中加入 NaA、NaB溶液,当两种沉淀共存时,依据溶度积常数判断AgB的溶解度小于AgA溶解度,AgA(s)?Ag+(aq)+A-(aq)、AgB(s)?Ag+(aq)+B-(aq);所以=$\frac{c({A}^{-})}{c({B}^{-})}$=$\frac{Ksp(AgA)}{Ksp(AgB)}$=$\frac{2.1×1{0}^{-10}}{1.0×1{0}^{-2}}$=2.1×10-8;
故答案为:2.1×10-8.
点评 本题涉及盐的水解原理、以及应用知识,属于综合知识的考查,难度不大.

| A. | 直接排放工业废气 | B. | 改进汽车尾气净化技术 | ||
| C. | 采用焚烧方法处理垃圾 | D. | 过度开采和使用化石燃料 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 最外层电子数呈周期性变化 | B. | 元素的相对原子质量逐渐增大 | ||
| C. | 核电荷数逐渐增大 | D. | 核外电子排布呈周期性变化 |
| A. | 将纯水加热至较高温度,Kw变大、pH变小、呈酸性 | |
| B. | 保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 | |
| C. | 向0.1 mol•L-1 氨水中加入少量水,pH减小,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| D. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
| A. | 在负极上发生氧化反应 | B. | 化学性质较活泼的金属为负极 | ||
| C. | 在外电路上电子由负极流向正极 | D. | 是由电能转化为化学能的装置 |
| A. | 臭氧 | B. | 氯气 | C. | 漂白粉 | D. | 明矾 |
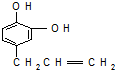

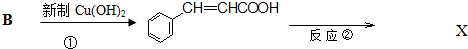
 .反应①的化学方程式为:
.反应①的化学方程式为: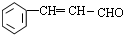 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$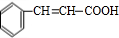 +Cu2O+2H2O.
+Cu2O+2H2O.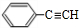 $→_{催化剂}^{HCl}$
$→_{催化剂}^{HCl}$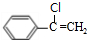 $→_{一定条件}^{CO、H_{2}}$
$→_{一定条件}^{CO、H_{2}}$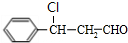 $→_{△}^{NaOH/醇}$
$→_{△}^{NaOH/醇}$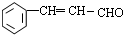 .
.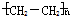
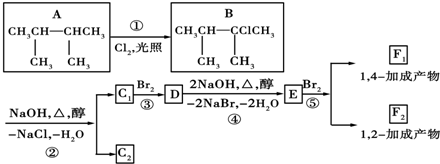
 .
. ;F1的结构简式是
;F1的结构简式是 .F1与F2的关系为同分异构体.
.F1与F2的关系为同分异构体.