题目内容
一个真空恒容密闭容器中盛有2mol PCl5,加热到200℃发生了反应PCl5(g)?PCl3(g)+Cl2(g),
反应达到平衡时PCl5的分解率为a%.若在同一温度下和同样容器中最初投入的是1mol PCl5,反应达到平衡时PCl5的分解率为b%,a与b的关系是( )
反应达到平衡时PCl5的分解率为a%.若在同一温度下和同样容器中最初投入的是1mol PCl5,反应达到平衡时PCl5的分解率为b%,a与b的关系是( )
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
考点:化学平衡的计算
专题:
分析:开始加入2molPCl5所到达的平衡,可以等效为先将体积增大1倍到达的平衡状态,该状态与开始加入1molPCl5是完全相同的平衡状态,然后在将体积压缩恢复到原来的体积,增大压强平衡向体积减小的方向移动,据此判断.
解答:
解:开始加入2molPCl5所到达的平衡,可以等效为先将体积增大1倍到达的平衡状态,该状态与开始加入1molPCl5是完全相同的平衡状态,然后在将体积压缩恢复到原来的体积,增大压强平衡向体积减小的方向移动,即平衡向逆反应方向移动,PCl5的分解率减小,故a%>b%,
故选B.
故选B.
点评:本题考查等效平衡,难度中等,关键是设计平衡建立的途径,可以直接等效为增大压强.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 |
| B、常温下,向Mg(OH)2饱和溶液中加入NaOH溶液,Mg(OH)2的Ksp不变 |
| C、带有“盐桥”的铜锌原电池比不带“盐桥”的铜锌原电池电流持续时间长 |
| D、对滴加酚酞的NaHCO3溶液加热,红色加深,是因为加热时NaHCO3分解生成Na2CO3,碱性增强 |
升高温度对CH3COOH的电离平衡、FeCl3的水解平衡、AgCl的溶解平衡的影响分别是( )
| A、促进、促进、促进 |
| B、抑制、抑制、促进 |
| C、促进、抑制、抑制 |
| D、抑制、促进、抑制 |
下列实验的相关描述正确的是( )

| A、快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法 |
| B、常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液 |
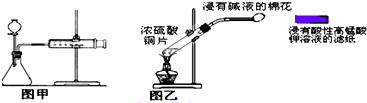
| C、甲装置可用于某些化学反应速率的测定.该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离,然后松手,观察针筒是否能回到原来刻度处 |
| D、乙装置可用来制取和检验二氧化硫气体漂白性,待滤纸颜色褪去后立即用浸有碱液的棉花堵住试管口 |
将BaO2放入密闭真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡时,下列说法正确的是( )
| A、平衡常数减小 |
| B、BaO量不变 |
| C、氧气浓度增大 |
| D、BaO2量增加 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.下列说法不正确的是( )
| A、淀粉和纤维素均可用(C6H10O5)n表示 |
| B、淀粉水解的最终产物能发生银境反应 |
| C、向蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水 |
| D、脂肪能溶于水 |
T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )


| A、在t1min时,3V正(B)=2V逆(C) |
| B、(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、T℃时,在相同容器中,若由0.3mol?L-1A、0.1 mol?L-1 B和0.4 mol?L-1 C反应,达到平衡后,C的浓度仍为0.4 mol?L-1 |
| D、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
大气污染指( )
| A、大气中含有少量的有毒、有害的物质 |
| B、大气中有毒、有害的物质可以自净到正常值 |
| C、大气中某些有毒、有害物质的含量超过正常值或大气的自净能力 |
| D、空气中氮气的含量大于氧气的含量 |