题目内容
2.3.6g烃A和Cl2发生取代反应,控制条件使其生成一氯代物,将反应生成的气体用NaOH溶液中和恰好和0.1mol•L-1NaOH溶液500mL完全反应,试解答下列问题:(1)求链烃A的相对分子质量72.
(2)若A既不能使酸性KMnO4溶液褪色又不能使溴水褪色,试求该烃的分子式C5H12,并写出符合该分子式的所有可能的同分异构体的结构简式CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4.
(3)若A的一氯代物只有一种,试确定A的结构简式并用系统命名法命名C(CH3)4、2,2-二甲基丙烷.
分析 设一氯代烃为R-Cl,与氢氧化钠发生反应:R-Cl+NaOH$→_{△}^{水}$R-OH+NaCl,反应消耗NaOH为0.5L×0.1mol/L=0.05mol,则一氯代烃的物质的量为0.05mol,故烃A的物质的量为0.05mol,则烃A的相对分子质量为$\frac{3.6}{0.05}$=72,由于$\frac{74}{14}$=5…2,属于烷烃,故烃A的分子式为C5H12,若烃的一氯代物只有一种,该烃分子中只有一种氢原子,故为新戊烷.
解答 解:(1)设一氯代烃为R-Cl,与氢氧化钠发生反应:R-Cl+NaOH$→_{△}^{水}$R-OH+NaCl,反应消耗NaOH为0.5L×0.1mol/L=0.05mol,则一氯代烃的物质的量为0.05mol,故烃A的物质的量为0.05mol,则烃A的相对分子质量为$\frac{3.6}{0.05}$=72,
故答案为:72;
(2)由于$\frac{74}{14}$=5…2,属于烷烃,故烃A的分子式为C5H12,可能结构简式有:CH3CH2CH2CH2CH3,CH3CH2CH(CH3)2,C(CH3)4,
故答案为:C5H12;CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4;
(3)若烃A的一氯代物只有一种,该烃分子中只有一种氢原子,故结构简式为C(CH3)4,名称为2,2-二甲基丙烷,
故答案为:C(CH3)4;2,2-二甲基丙烷.
点评 本题考查有机物推断,注意结合相对分子质量利用商除法确定分子式,掌握有机物命名,难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
12.用惰性电极电解下列溶液时在阴极有固体析出,在阳极有气泡产生的是( )
| A. | H2SO4 | B. | CuSO4 | C. | NaCl | D. | KOH |
13.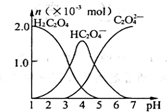 常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
( )
 常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是( )
| A. | HC2O4-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=10 mL,时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=15 mL,时,溶液中存在:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=20 mL,时,溶液中存在:c(OH-)=c(HC2O4-)+2c(H2C2O4)+c(H+) |
10.盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象.某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案.请回答有关问题.
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
则x=7.
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
| 编号 | 盐酸 | 氢氧化钠 | △t/℃ |
| 1 | 0.1mol•L-1 | 0.05mol•L-1 | 3.5 |
| 2 | 0.1mol•L-1 | 0.1mol•L-1 | x |
| 3 | 0.2mol•L-1 | 0.2mol•L-1 | 14 |
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.
17.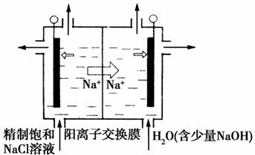 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为0.1mol.
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
7.下列反应的离子方程式正确的是( )
| A. | 硫酸铜与烧碱溶液反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 碳酸钠溶液中加入足量盐酸:Na2CO3+2H+═Na++CO2↑+H2O | |
| D. | 氢氧化铝中和胃酸(盐酸):Al(OH)3+3H+═Al3++3H2O |
 ;
;