题目内容
11.2.00gC2H2完全燃烧生成液态水和CO2,放出99.6KJ的热量,则3mol C2H2完全燃烧能放出多少热量?分析 根据2.00g C2H2气体完全燃烧生成液态水和CO2,放出99.6kJ的热量,由物质的量之比等于热量比计算3molC2H2燃烧放出的热量.
解答 解:2.00g C2H2气体完全燃烧生成液态水和CO2气体,放出99.6kJ的热量,则3molC2H2气体完全燃烧放出的热量为$\frac{3mol×26g/mol}{2g}$×99.6kJ=3884.4kJ,
答:3mol C2H2完全燃烧能放出3884.4kJ热量.
点评 本题考查了反应热的计算,题目难度不大,注意反应热与物质之间的关系计算,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
19.某核素${\;}_{Z}^{A}X$可形成HmX型氢化物,则 a g HmX 含有( )
| A. | $\frac{a}{A+m}(Z+m)$mol质子 | B. | $\frac{a}{A}(Z+m)$mol电子 | ||
| C. | $\frac{a}{A+m}(A-Z+m)$mol中子 | D. | $\frac{a}{A}$mmol HmX |
16.在某些工厂中常用高压电对气溶胶作用来除去大量的烟尘.以减少污染,这种做法所应用的原理是( )
| A. | 电泳 | B. | 胶体的聚沉 | C. | 布朗运动 | D. | 电解 |
3.在一定条件下,下列选项中括号内的物质能被完全消耗的是( )
| A. | 常温下将64g铜片投人过量浓硫酸中(铜片) | |
| B. | 向含有0.2molBa(OH)2和O.lmolNaOH的混合溶液中通人标况下3.36LCO2(CO2) | |
| C. | 向lOmL3mol•L-1的盐酸中加人5.6g铁(铁) | |
| D. | 向5.5gMn02粉末中加人20mL2mol•L-1双氧水(Mn02) |
1.用电解的方法可除去溶液中的NO3-,其原理如图所示,下列说法中正确的是( )
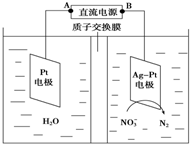

| A. | 铅蓄电池的B极为正极,电极材料为PbO2 | |
| B. | 铅蓄电池工作过程中负极质量增加 | |
| C. | 该电解池的阳极反应为:2 NO3-+6H2O-10e-═N2↑+12OH- | |
| D. | 若电解过程中转移10mol电子,则生成N2的体积为22.4L |
 ⑤
⑤ ⑧
⑧ ⑨
⑨ .
.