题目内容
7.将少量金属钠分别投入下列物质中,有气体放出,且溶液质量减轻的是( )| A. | H2SO4 | B. | CuSO4 | C. | KNO3 | D. | KOH |
分析 钠和水反应生成氢氧化钠和氢气,会出现气体,如果溶液质量减轻,则说明从溶液中放出气体的质量大于溶液增加的质量,根据金属钠和下列物质间的反应情况来回答;
解答 解:A、钠和H2SO4的反应方程式为:2Na+H2SO4═Na2SO4+H2↑,根据方程式知,溶液增加的质量=m(Na)-m(H2),故A错误;
B、钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,生成的氢氧化钠和硫酸铜反应,方程式为:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,将两个方程式相加:2Na+2H2O+CuSO4═H2↑+Na2SO4+Cu(OH)2↓,由方程式知,溶液的质量减轻,故B正确;
C、将金属钠加入到硝酸钾溶液中,只有金属钠和水之间反应,钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,根据方程式知,溶液增加的质量=m(Na)-m(H2),故C错误;
D、钠与氢氧化钾反应,也就是钠和水的反应方程式为:2Na+2H2O═2NaOH+H2↑,所以溶液质量增加,溶液增加的质量=m(Na)-m(H2),故D错误;
故选:B.
点评 本题考查了钠及氢氧化钠的性质,难度不大,注意根据方程式运用差量法分析反应后溶液质量的变化即可.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
10.下列化学方程式中,属于水解反应的是( )
| A. | CH3COOH+H2O?CH3COO-+H3O+ | B. | HS-+H2O?S2-+H3O+ | ||
| C. | CO2+H2O?HCO3-+H+ | D. | CO32-+H2O?HCO3-+OH- |
11.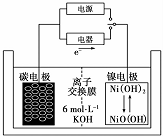 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为原电池的负极 | |
| D. | 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O |
8.下列说法正确的是( )
| A. | 油脂属于天然高分子化合物,在碱性条件下水解可制得肥皂 | |
| B. | 在一定条件下,氨基酸之间能发生反应合成多肽 | |
| C. | 在淀粉水解液中加入氢氧化钠,再加入碘水,溶液未变蓝,说明淀粉己完全水解 | |
| D. | 蛋白质溶液中加入Na2SO4浓溶液有固体析出,加入足量水后固体不溶解 |
2.配制200mL 0.100mol•L-1盐酸溶液时,下列实验操作使所配的溶液浓度偏大的是( )
| A. | 用量筒量取所需的浓盐酸时仰视读数 | |
| B. | 用量筒量取的浓盐酸时,量筒里有少许蒸馏水 | |
| C. | 定容时,仰视标线 | |
| D. | 定容后倒转容量瓶数次摇匀,发现液面最低点低于标线,再补加几滴蒸馏水至标线 |
12.实验室里可按如图所示的装置干燥、储存气体 R,多余的气体可用水吸收,则 R是( )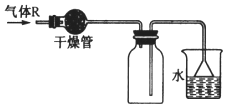

| A. | NO2 | B. | HCl | C. | SO2 | D. | NH3 |
19.已知(1)H2O(g)=H2O(l)△H1=-Q1 kJ•mol-1
(2)CH3OH(g)=CH3OH(l)△H2=-Q2 kJ•mol-1
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H3=-Q3 kJ•mol-1
(Q1、Q2、Q3均大于0)若使1mol液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)( )
(2)CH3OH(g)=CH3OH(l)△H2=-Q2 kJ•mol-1
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H3=-Q3 kJ•mol-1
(Q1、Q2、Q3均大于0)若使1mol液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)( )
| A. | Q1+Q2+Q3 | B. | 0.5Q3-Q2+2Q1 | C. | Q3-2Q2+4Q1 | D. | 0.5(Q1+Q2+Q3) |
16.已知反应:
①2CH3OH(g)?CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7kJ/mol
在C2H4(g)+H2O(g)=CH3CH2OH(g)△H4中,△H4等于( )
①2CH3OH(g)?CH3OCH3(g)+H2O(g)△H1=-23.9kJ/mol
②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ/mol
③CH3CH2OH(g)═CH3OCH3(g)△H3=+50.7kJ/mol
在C2H4(g)+H2O(g)=CH3CH2OH(g)△H4中,△H4等于( )
| A. | -48.5kJ/mol | B. | +48.5kJ/mol | C. | -45.5kJ/mol | D. | +45.5kJ/mol |
17.以NA表示阿佛加德罗常数,下列说法中正确的是( )
| A. | 78g过氧化钠中含2NA个O2- | |
| B. | 0.1molOH-含NA个电子 | |
| C. | 1.8g重水(D2O)中含NA个中子 | |
| D. | 标准状况下11.2L臭氧中含NA个氧原子 |