题目内容
11.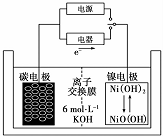 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为原电池的负极 | |
| D. | 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O |
分析 根据图片中电子流向知,放电时,石墨电极是负极,电极反应式为H2+2OH--2e-=2H2O,正极反应式为NiO(OH)+H2O+e-═Ni(OH)2+OH-,充电时阴阳极与放电时负极、正极反应式正好相反,以此解答该题.
解答 解:A.充电时,阴极上得电子发生还原反应,故A错误;
B.充电时,C电极作阴极,所以应该与电源负极相连,故B错误;
C.由电子流向可知,放电时,石墨电极是负极,发生氧化反应,故C正确;
D.放电时镍电极是正极,正极上得电子发生还原反应,电极反应式为NiO(OH)+H2O+e-═Ni(OH)2+OH-,故D错误.
故选C.
点评 本题考查化学电源新型电池,为高考高频点,侧重考查学生的分析能力,明确各个电极上发生的反应是解本题关键,会结合电解质溶液酸碱性书写电极反应式,知道放电时和充电时电极反应式关系,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
2.铁钉在下列情况下腐蚀最快的是( )
| A. | 铁钉放在干燥的空气中 | B. | 铁钉完全浸没在植物油中 | ||
| C. | 铁钉一半浸没在食盐水中 | D. | 铁钉一半浸没在水中 |
19.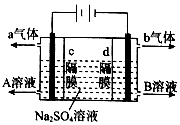 利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
 利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )
利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠.下列叙述正确的是( )| A. | a气体为氢气,b气体为氧气 | |
| B. | A为氢氧化钠溶液,B为硫酸溶液 | |
| C. | 通电后中间隔室的SO42-向阴极移动,阳极区溶液的pH增大 | |
| D. | 该电解反应的方程式为2Na2SO4+6H2O$\frac{\underline{\;电解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |
6.下列化学反应的离子方程式,书写不正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 向氯化铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 氯化亚铁溶液中通入少量氯气:Cl2+2Fe2+═2Fe3++2Cl- | |
| D. | 往明矾溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++2SO42-+Al3++4OH-═2BaSO4↓+AlO2-+2H2O |
16.下列物质属于非电解质的是( )
| A. | 液氯 | B. | 酒精 | C. | 氯化钠 | D. | 水 |
3.下列说法正确的是( )
| A. | 使用容量瓶配制溶液时,应先检漏 | |
| B. | 用焰色反应鉴别NaCl固体和NaOH固体 | |
| C. | 用丁达尔效应鉴别NaCl溶液和KCl溶液 | |
| D. | 蒸馏操作时,应使温度计水银球插入混合溶液的液面下 |
7.将少量金属钠分别投入下列物质中,有气体放出,且溶液质量减轻的是( )
| A. | H2SO4 | B. | CuSO4 | C. | KNO3 | D. | KOH |
8.下列说法错误的是( )
| A. | 酸雨形成的主要原因是大量石油、煤等矿物燃料的燃烧 | |
| B. | 反应物的总能量高于生成物的总能量时,反应放热 | |
| C. | 原电池是化学能转变为电能的一种装置 | |
| D. | 在铜、锌和稀硫酸构成的原电池中,铜是负极 |
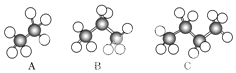 (1)如图是几种烷烃的球模型,试回答问题:
(1)如图是几种烷烃的球模型,试回答问题: .
.