题目内容
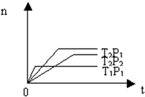 反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )
反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )| A、T1<T2,P1<P2 |
| B、T1<T2,P1>P2 |
| C、T1>T2,P1>P2 |
| D、T1>T2,P1<P2 |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:根据温度、压强对平衡移动的影响分析,温度越高、压强越大,则反应速率越大,达到平衡用的时间越少,曲线的斜率越大.
解答:
解:根据温度对反应速率的影响可知,温度越高,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:T1>T2;
根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:P1>P2,
故选C.
根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:P1>P2,
故选C.
点评:本题考查化学平衡图象题,题目难度中等,注意温度、压强对反应速率和化学平衡的影响.

练习册系列答案
相关题目
下列相关反应的离子方程式书写正确的是( )
| A、氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、硫酸铜溶液显酸性:Cu2++2H2O═Cu(OH)2↓+2H+ |
| C、向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-=NH3↑+H2O |
| D、用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
下列物质中,属于酸酐的是( )
| A、NO2 |
| B、CO |
| C、SO2 |
| D、CuO |
已知下列热化学方程式:H2(g)+
O2(g)═H2O(l)△H=-285.8kJ/mol,H2(g)+
O2(g)═H2O(g)△H=-241.8kJ/mol则氢气的标准燃烧热是( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、-285.8kJ/mol |
| B、285.8kJ/mol |
| C、-241.8kJ/mol |
| D、241.8kJ/mol |
实验室中需要配制2mol?L-1的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、950 mL,111.2 g |
| B、500 mL,117 g |
| C、1 000 mL,117 g |
| D、1 000 mL,111.2 g |
溴乙烷与氢氧化钾溶液共热,既可生成乙烯又可生成乙醇,其条件区别是( )
| A、生成乙烯的是热的氢氧化钾的水溶液 |
| B、生成乙醇的是热的氢氧化钾的水溶液 |
| C、生成乙烯的是在170℃下进行的 |
| D、生成乙醇的是热的氢氧化钾的醇溶液 |

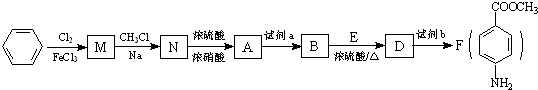
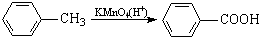


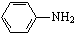 最多能够和
最多能够和 结构;
结构;