题目内容
30mL某气体NxHy全部分解生成30mLN2和60mLH2,上述气体的体积均在同温同压的条件下测定.由此推断该气体的摩尔质量是 .
考点:摩尔质量
专题:计算题
分析:在同温同压下,气体的物质的量之比等于气体的体积之比,根据反应的原子守恒得出NxHy的化学式,而一种物质的摩尔质量在数值上等于该物质的相对分子质量.
解答:
解:在同温同压下,气体的物质的量之比等于气体的体积之比,故反应的化学方程式为:NxHy=N2+2H2,根据原子守恒,可知X=2,Y=4,故化学式为:N2H4,相对分子质量为32,故摩尔质量为32g/mol,故答案为:32g/mol.
点评:本题考查了物质的摩尔质量的求算,根据气体的体积等于物质的量之比和原子守恒来计算.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
实现下列变化需要加入还原剂才能实现的是( )
| A、Fe2O3→Fe |
| B、Cu→Cu(NO3)2 |
| C、SO3→H2SO4 |
| D、KClO3→KCl |
下列仪器的主要成分不属于硅酸盐材料的是( )
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
| A、③④⑤ | B、②④⑤ |
| C、①③⑤ | D、②③④ |
下列说法正确的是( )
| A、摩尔质量就是该物质的相对分子质量 |
| B、6.02×1023即是阿伏伽德罗常数 |
| C、标准状态下,1mol水的体积约为22.4L |
| D、同温,同压下,1molAI和1molH2SO4(液体)的体积不相等 |
短周期主族元素X、Y、Z、W的原子序数依次递增.X的原子核中无中子;Y原子最外层电子数是内层的2倍;Z、W为同族元素,形成的WZ2分子是酸雨的主要成因.下列说法中正确的是( )
| A、X与Y形成原子个数比为1:1的化合物只有两种 |
| B、Y、W的氧化物均为酸性氧化物 |
| C、最高价氧化物对应水化物的酸性Y<W |
| D、X与Z形成的化合物中,各原子均满足8电子稳定结构 |
将V升CO和H2的混合气体充分燃烧,需相同条件下0.5V的O2则CO和H2的体积比是( )
| A、1:1 | B、2:1 |
| C、1:2 | D、任意比 |
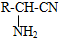 ,R-CN
,R-CN
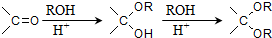 ,写出由乙烯、甲醇为有机原料制备化合物
,写出由乙烯、甲醇为有机原料制备化合物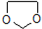 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH3CH2OH