题目内容
实现下列变化需要加入还原剂才能实现的是( )
| A、Fe2O3→Fe |
| B、Cu→Cu(NO3)2 |
| C、SO3→H2SO4 |
| D、KClO3→KCl |
考点:氧化还原反应
专题:氧化还原反应专题
分析:需要加入还原剂才能实现,则选项中氧化剂在反应中元素的化合价降低,以此来解答.
解答:
解:A.Fe元素化合价降低,被还原,应加入还原剂,故A正确;
B.Cu元素化合价升高,被氧化,应加入氧化剂,故B错误;
C.元素化合价没有发生变化,不是氧化还原反应,故C错误;
D.Cl元素化合价降低,但无需加入还原剂,可在二氧化锰催化作用下分解,故D错误.
故选A.
B.Cu元素化合价升高,被氧化,应加入氧化剂,故B错误;
C.元素化合价没有发生变化,不是氧化还原反应,故C错误;
D.Cl元素化合价降低,但无需加入还原剂,可在二氧化锰催化作用下分解,故D错误.
故选A.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化解答的关键,侧重还原反应的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案
相关题目
在下述条件下,一定能大量共存的离子组是( )
| A、无色透明的水溶液中:K+、Ba2+、I-、MnO4- |
| B、c(HCO3-)=0.1mol?L-1的溶液中:Na+、K+、CO32-、Br- |
| C、含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ |
| D、强碱性溶液中:HCO3-、K+、C1-、Na+ |
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:N2O4?2NO2 △H>0,在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码.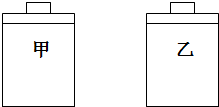
(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码.

| A、(a)甲>乙,(b)甲>乙 |
| B、(a)甲>乙,(b)甲=乙 |
| C、(a)甲<乙,(b)甲>乙 |
| D、(a)甲>乙,(b)甲<乙 |
 A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )
A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )| A、0.054g |
| B、0.108g |
| C、0.216 |
| D、0.432g |
下列关于反应热的说法正确的是( )
| A、当△H为负值时,表示该反应为吸热反应 |
| B、燃烧不一定是放热反应 |
| C、反应热的大小与反应物所具有的能量和生成物具有的能量无关 |
| D、反应热的大小只与反应体系的始态和终态有关 |
将质量分数为a%的乙醇溶液和质量分数为(1-a)%的乙醇溶液等体积混合后所得乙醇溶液的质量分数可能是( )
| A、大于50% |
| B、小于50% |
| C、小于或等于50% |
| D、大于或等于50% |
设NA为阿伏加德罗常数,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、16 g CH4所含原子数目为NA |
| C、17 g NH3 所含氢原子数目为4 NA |
| D、18 g水所含分子数目为NA |
下列关于各物质的化学用语表达正确的是( )
A、四氯化碳的电子式: |
B、丙烷分子的比例模型: |
C、环己烷的结构简式: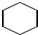 |
| D、乙酸的分子式:CH3COOH |